【英文名称】Sodium Hydride
【分子式】NaH
【分子量】24.00
【 CA 登录号】7646-69-7
【物理性质】灰色粉末,mp 800°C,d 1.396 g/cm3。氢化钠在所有的有机溶剂中都不溶,也不溶于液氨;但溶于熔化的钠,遇水剧烈分解。
【制备和商品】国内外试剂公司均有销售,商品试剂为松散的灰色粉末( 95 %的干燥氢化物)或是分布在矿物油中的灰色粉末分散物。
【注意事项】(1)该试剂的矿物油分散物是固体,可以在空气中取用;分散物和戊烷混合搅拌可以从中除去矿物油,氢化物下沉,用移液管吸去浮在表面上的戊烷 / 矿物油。但是,在吸取前应用少量的乙醇处理上层清液,以避免氢化物被吸走。干燥的固体应保存在惰性气体中。
( 2 )氢化钠粉粒是剧烈的刺激物,因此,所有的操作都应在干燥的环境和通风橱中进行。氢化钠在温度低于 230 ° C 的干燥空气中是稳定的,到230°C时发生燃烧。在潮湿的空气中,氢化钠迅速分解,如杲是纯的粉末,水解产生的热量能导致自燃。氢化钠比金属钠更容易与水反应,反应产生的热量可使氢气燃烧。
氢化钠( NaH )作为强碱参与多种反应,能与氧、氮、碳和锗/硅有机酸反应,或者与其它化合物组成催化剂。氢化钠还是一种还原剂和溶剂干燥剂。
与 O-有机酸反应 氢化钠可以促进分子内的酯交换反应。Su等人在㈠-Apicularen A的全合成中,将化合物1与氢化钠在四氢呋喃中回流,酯交换反应后得到大环内酯类化合物2(式1)[1]。
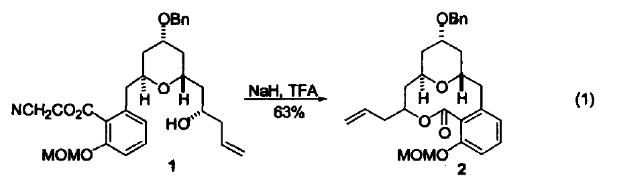
与N-有机酸反应 在 NaH 和催化量的水存在下,化合物 3 与Me2SO4 在 TFA 中反应 30 min 得到化合物4(式2)[2]。氢化钠与催化量的水反应生成高活性的氢氧化钠,从而使反应速率加快,收率提高。一分钟内反应基本完成,比直接用粉末状的氢氧化钠快很多。此方法不失为氨基酸及其类似物甲基化的有效方法。
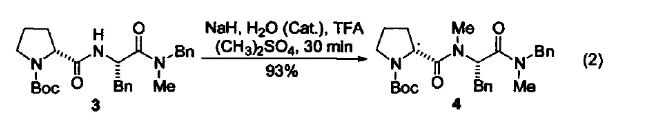
与C-有机酸反应 在 Ullmann 偶合反应中,氢化钠作为强碱与NiCl2(PPh3)2、PPh3、Zn、甲苯组成的催化系统可以得到高产率的偶联产物(式3)[3]。用氢化钠脱卤化氢是形成亚甲基的好方法[4]。
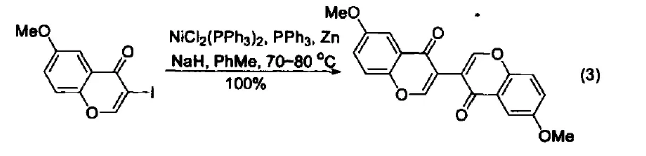
与 Ge/Si 有机酸反应 在醚溶剂中,Ge-H键和Si-H键可以被氢化钠切断[ 5 ]。高温下,氢化钠还可以把 Si-O 键转变成 Si-C 键(式4)[6],这是把Si-O键转变成Si-C键的一种方便和快捷的方法。
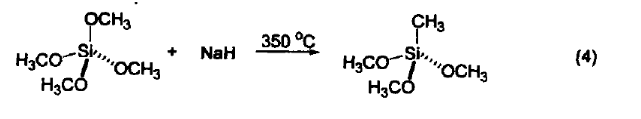
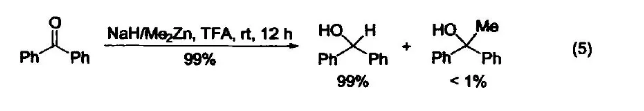
作为还原剂NaH和Me2Zn组成的还原剂复合物可以把酯、氨基化合物、醛、酮还原成为相应的醇和胺。还可以高选择性地对α,β-不饱和羰基化合物进行1,2-还原,使环氧化合物立体选择性幵环。在酮存在时,可以实现化学选择性地还原醛。在还原剂复合物中,氢化钠作为 Lewis 碱,Me2Zn 作为 Lewis 酸,二者在溶剂 TFA 中形成复合物。此还原剂复合物的选择性很好(式5),是一种很好的将醛、酮还原成醇的方法[7]。
参考文献
1. Su, Q. B.; Panek, J. S.J. Am. Chem. Soc. 2004, 126,2425.
2. Prashad, M.;HarD.; Hu, B.; Kim, H. Y.; Repic, O.; Blacklock, T. J. Org. Lett. 2003,5, 125.
3. Lin, G. Q.; Hong, R. J. Org. Chem. 2001,66, 2877.
4. Khan, K. M.; PeTvecn, S.; Shah, S. T. A.; Shekhani, M. S.; Voelter, W. New J. Chem. 2001, 25, 896.
5. Corriu, R. J. P.; Guerin, C.J. Organomet. Chem. 1980,197, 19.
6. Schattenmann, F. J.; Ligon, W. V.; Donahue, P.; Grade, H.; Abatto, K. Organometallics 2004, 23, 6202.
7. Uchiyama, M.; Furumoto, S.; Saito, M.; Kondo, Y.; Sakamoto, T. J. Am. Chem. Soc. 1997, 119, 11425.
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 2 Qiande Road, Life Science High Tech Zone, Jiang Ning District, Nanjing, Jiangsu Province, China