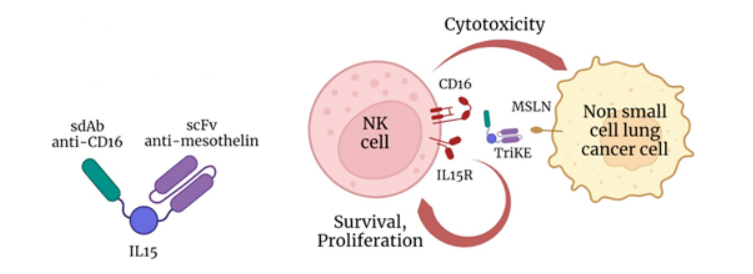
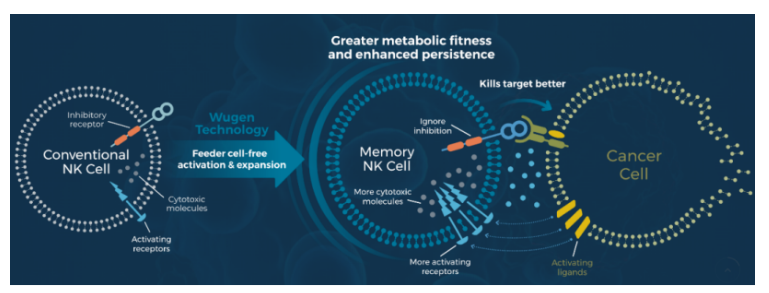
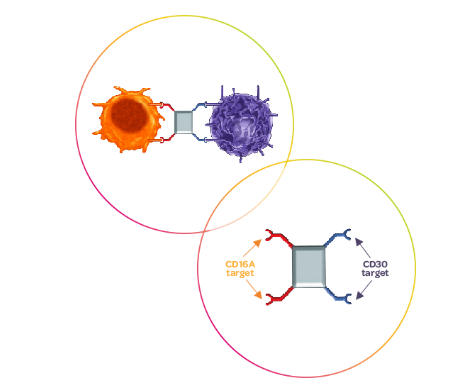
据统计,当前NK细胞疗法多数大多处于临床前或者临床研究早期阶段。不过,从已经公布的数据来看,基于NK细胞的免疫疗法可以被分为各具特点与优势五个大类,采取不同的治疗手段针对不同领域,具有广阔的市场前景。基于NK细胞的疗法根据注输的有效物质以及疗法生效的手段,可以将这些疗法分为非细胞疗法与细胞疗法。细胞因子疗法 通过注输细胞因子,可以激活患者体内的NK细胞,从而增强杀伤能力。例如,IL-2可以直接刺激T细胞和NK细胞的增生和激活,但在体内会受到毒副作用和激活免疫抑制性调节性T细胞(Treg)的限制,多家公司正在开发选择性激活T细胞和NK细胞的IL-2类似物。单抗疗法 NK细胞可以被IgG抗体激活,产生抗体依赖性细胞介导的细胞毒性(ADCC)。向患者体内注输抗体,可以针对性靶向NK细胞抑制受体来激活NK细胞,或是靶向肿瘤相关抗原,通过NK细胞诱导ADCC效应,通过CD16受体介导的ADCC可以杀死IgG1或IgG3抗体靶向的细胞。NK细胞接合器 细胞接合器可以同时靶向肿瘤细胞抗原以及NK细胞活化受体,通常是双特异性或者三特异性抗体,类似于T细胞接合器,将NK细胞与肿瘤细胞拉在一起来实现对肿瘤细胞的杀伤。过继性NK细胞疗法 这一疗法向患者注输的是健康的、经过细胞因子活化的NK细胞,通过不同渠道收集NK细胞,例如外周血NK细胞、来自脐带血或胎盘的NK细胞,以及从诱导多能干细胞(iPSC)分化生成的NK细胞,在体外增强功能后进行注输,从而增强患者体内的肿瘤杀伤能力。基因工程化NK细胞疗法 与过继性NK细胞疗法不同的是,这一治疗方法采取注输基因改造的NK细胞,包括CAR-NK细胞,从而实现针对性杀伤,增强其抗肿瘤效应。与CAR-T疗法相比,CAR-NK细胞具有细胞因子释放综合征风险更小等优势。基于CAR-T的成功,CAR-NK这一治疗手段的热度在逐年上升,国内外已经有多家企业布局CAR-NK疗法,并且针对其体外扩增难、转染效率低、细胞持久性较差等挑战开发创新性应对措施。2022年7月27日,临床阶段的生物技术公司Celularity宣布,NK细胞疗法CYNK-101的1/2a期临床试验已经完成了首例患者给药,该试验针对晚期HER2阳性胃或胃食管交界处(G/GEJ)癌症的一线治疗。CYNK-101是一种新型的同种异体现成人类胎盘CD34+干细胞衍生的NK细胞候选疗法,经过基因改造以表达高亲和抗裂解的CD16(FCGRIIIA)变体,从而增强抗体依赖的细胞介导的细胞毒性作用(ADCC)。2022年6月10日,免疫肿瘤公司GT Biopharma在第27届欧洲血液学大会上展示了关于慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)的临床前数据。数据表明,第二代CD19靶向三特异性杀伤接合器(TriKE®)GTB-7550可以驱动强大的NK细胞功能,以对抗B细胞恶性肿瘤。TriKE可以交联CD16/FcγRIII和NK细胞上的肿瘤抗原,能够驱动细胞毒性,而IL15为NK细胞提供存活和增殖信号。这一分子包括人源化骆驼抗CD16VHH单域抗体CAM16、野生型IL-15成分和抗CD19肿瘤抗原单链可变区片段(scFv),均通过短肽接头连接,可增强针对CD19+癌症靶点的NK杀伤功能。▲ GT Biopharma第二代接合器 图源:公司官网2022年6月10日,Wugen在2022年欧洲血液学协会(EHA)上展示了其领先NK细胞治疗产品WU-NK-101的最新临床前数据。与传统NK细胞相比,WU-NK-101表现出更强的代谢活性和对肿瘤微环境(TME)免疫抑制的抵抗力,其在急性髓性白血病(AML)的临床前模型中显示出强大的体外和体内抗肿瘤活性。WU-NK-101是利用其专有的MonetaTM平台所开发的同种异体记忆NK细胞疗法,具有独特的、更强效的抗肿瘤活性和细胞因子诱导的记忆样(CIML)表型,与传统的自然杀伤细胞(cNK)相比,具有更好的活化、代谢灵活性和细胞毒性。▲ Wugen通用型记忆NK细胞平台作用机理 图源:公司官网2022年4月26日,Nkarta公布了两款CAR-NK在研管线NKX101和NKX019治疗血液瘤的最新临床数据,这是Nkarta公司首次公布其CAR-NK研发项目的临床试验结果。NKX101和NKX019是两款同种异体的即用型NK细胞疗法,使用外周血来源NK细胞。NKX101是Nkarta的首发管线,是一种病毒转染工程化的靶向NKG2D配体的异体CAR-NK细胞产品,在治疗复发/难治性急性髓系白血病(AML)和骨髓增生异常综合症(MDS)的临床试验中,高剂量组5名AML患者中3名获得完全缓解(60% CR),其中两例是MRD微小残留病灶阴性,显示了NKX101治疗AML良好的耐受性、安全性和高度活性。NKX019是一款靶向CD19的通用型CAR-NK细胞疗法,在治疗复发/难治性B细胞淋巴瘤的临床试验中,高剂量组6名患者中5名获得了部分缓解(83% ORR),其中3名获得了完全缓解(50% CR),CR病例中包括一名弥漫性大B细胞淋巴瘤患者和一名套细胞瘤患者,试验中并未发现剂量限制性毒性和细胞因子风暴。➤ 2022年4月10日,Affimed在AACR会议上展示了NK细胞衔接器ICE®疗法AFM13预混脐带血来源的NK细胞疗法的临床数据。数据显示,在接受AFM13的2期临床推荐剂量(RP2D)的所有13名患者中,客观缓解率为100%,完全缓解率从接受第一疗程治疗后的38%提高到两个疗程后的62%。AFM13是一款first-in-class双特异性四价抗体,即先天性细胞接合器ICE®,通过独特的设计,可以使其与NK细胞和巨噬细胞上的CD16A和淋巴瘤细胞上的CD30高亲和力结合,从而将NK细胞和巨噬细胞募集到肿瘤细胞附近,并且激活它们杀死肿瘤细胞。AFM13还结合了脐带血来源的NK细胞疗法,旨在加强ADCC作用。目前,NK细胞疗法在很多地方都在模仿相对成熟的T细胞疗法,例如CAR结构的构建以及转染,但相对T细胞疗法而言,NK细胞疗法具有以下几个优势:更广泛的细胞来源,更广泛的适应症,更多的杀伤途径,更好的安全性以及可作为通用型现货产品。虽然近年来基于NK细胞的免疫疗法取得了不少突破,但大多候选药物仍处于较为早期的阶段。根据初步的数据可以看到这一治疗方案的有效性与安全性,也可以预测出这一领域的未来前景。随着CARs、先进抗体工程学以及多元受体结合技术的发展,基于NK细胞的免疫疗法毫无疑问将在未来有值得期待的临床进展。1.Maskalenko et al., (2022). Harnessing natural killer cells for cancer immunotherapy: dispatching the first responders. Nature Reviews Drug Discovery, https://doi.org/10.1038/s41573-022-00413-7