在人类幻想世界中,战胜疾病、科幻进化的最终手段往往都来自“基因”,自1996年人类历史上第一只克隆生物克隆羊多利诞生之后,包括《千钧一发》《第六日》等电影作品的推出 ,让基因技术类科幻片迎来 了属于自己的小高潮,也让大众对基因技术这个全新技术有了意想层面的认识。
但谁曾想,短短十数年间的科学技术发展,基因疗法早已不再是想象中的技术,而是逐渐走入了我们的现实生活,开始服务于各种“罕见病新药”研发。
据参考资料显示,约80%罕见病是源于基因缺陷而导致的遗传病,其中单基因病比例最高。而所谓基因疗法,是指利用载体将遗传物质引入靶细胞,通过纠正或补充缺陷基因来治疗或预防疾病,而该项技术的最佳应用场景又正是单基因疾病。
两者匹配之下,基因疗法与罕见病恰好相得益彰,基因疗法成为了罕见病治疗的全新力量。
另外,由于在目前已知的7000多种罕见病中,超过95%的疾病并无FDA批准的针对性药物,常规治疗方法多是对症治疗与替代治疗,但这些方法只能缓解症状,并不能根治病因,且可能还伴随一定程度的副作用和风险。如血友病的凝血因子治疗、DMD的糖皮质激素治疗等等。所以,最终导致罕见病临床上对病因调控类型药物的需求长期存在,相关的支付意愿也相对较高。
基因疗法的出现,不同于传统小分子药物和抗体药物在蛋白质水平进行调控,其可以在DNA或mRNA水平上对致病基因进行修正从而达到治疗效果,既克服传统小分子和抗体的不足,对于致病基因清晰的罕见病几乎可以做到,将症状治疗完全转变成为病因治疗,一劳永逸,应用空间巨大,对于罕见病治疗更是具有“划时代”意义。
虽不能说基因疗法只能应用于罕见病领域,毕竟肿瘤、代谢、慢病领域已经开始出现了基因疗法的具体应用,未来的基因疗法甚至大概率将与生活中的常规疾病结合,比如前段时间,Fractyl Health展示的其“Rejuva基因治疗平台”的临床前研究成果,利用腺相关病毒(AAV)载体实现“一次给药持久减重”,单剂输注后28天,将小鼠体重降低27%,高于了对照组持续司美格鲁肽治疗的21%数据。
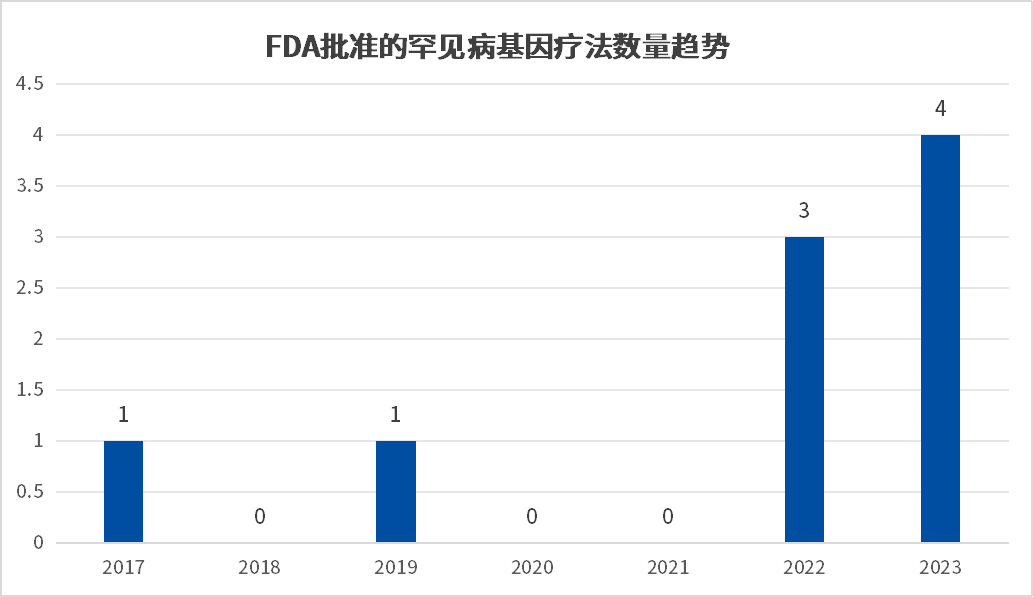
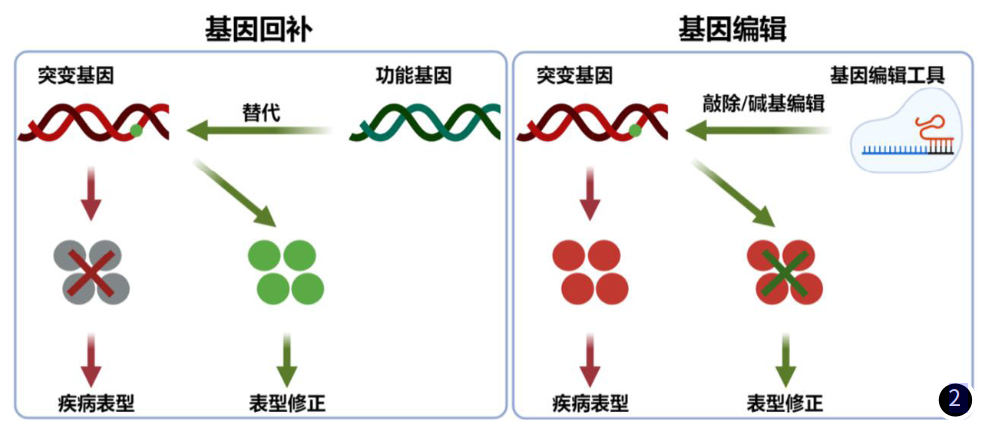
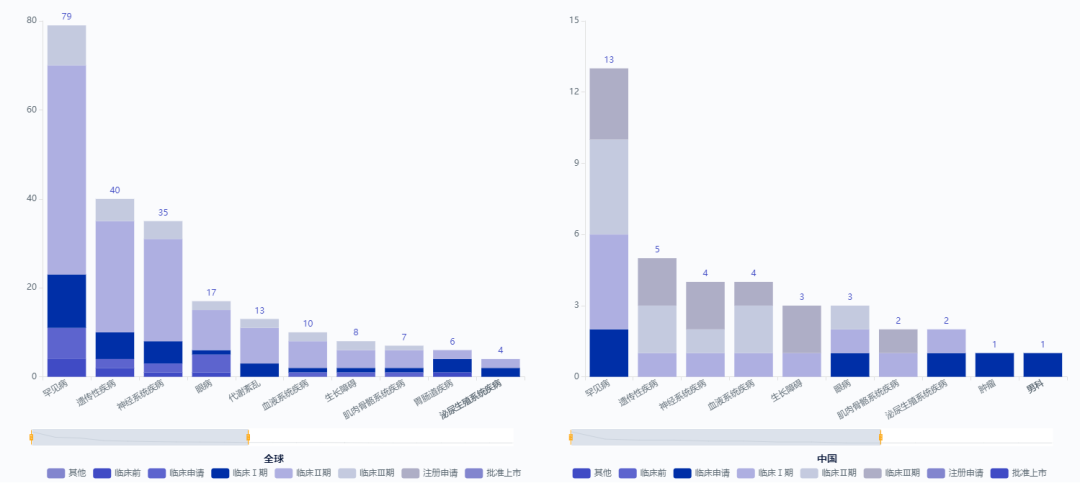
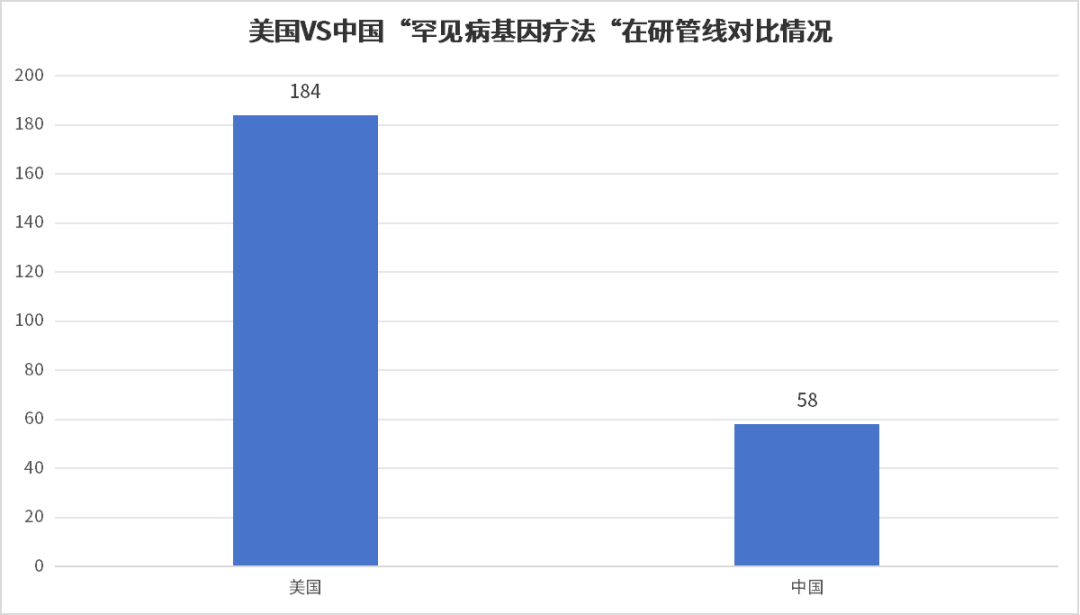
适应症为“罕见病” 2023年,美国FDA批准新药中,包含了5款全新的基因疗法,且其中4款亦选择了罕见病领域,分别是针对镰状细胞病(SCD)的Casgevy与Lyfgenia、针对A型血友病的Roctavian以及针对杜氏肌营养不良症(DMD)的Elevidys; 2017至今,历史获批的10款基因疗法中,更是有9款是针对的罕见病领域; 药品 适应症 获批时间 原研企业 市场预估 Casgevy 镰状细胞病(SCD) 2023年12月8日 39亿美元 Roctavian A型血友病 2023年6月29日 BioMarin Pharmaceutical 22亿美元 Elevidys 杜氏肌营养不良症(DMD) 2023年6月22日 Sarepta Therapeutics 10亿美元 Lyfgenia 镰状细胞病(SCD) 2023年12月8日 Bluebird bio 3.79亿美元(2029年) 基因回补与基因编辑同步进行 而一般情况下,罕见病的基因治疗大致策略可分为两者,一者是针对由特定基因缺陷引起的疾病,可通过递送缺失功能基因的正常版本来纠正,简称“基因回补”;二者是针对由错误折叠的毒性蛋白引起的疾病,可以通过递送基因编辑工具对突变基因进行敲除或纠正,简称“基因编辑”。 四大领域 罕见病基因疗法应用最广泛 凭借基因疗法在部分领域高转导效率等因素,据药智数据显示,79项目活跃管线(近一年有临床进展)中,血液系统、神经系统、肌肉骨骼与眼科罕见病领域是目前基因治疗应用最多的领域。 血液病领域 FDA批准的血液罕见病领域新药与其技术类型 药品名称 企业 技术类型 适应症 Casgevy Vertex Pharmaceuticals, Inc/CRISPR Therapeutics 基因编辑-CRISPR 输血依赖型β-地中海贫血(TDT)和镰刀状细胞贫血病(SCD) Lyfgenia bluebird bio, Inc. 镰状细胞病 (SCD) Roctavian BioMarin Pharmaceutical 基因递送-腺病毒载体(AAV) 血友病A Hemgenix CSL Behring LLC 基因递送-腺病毒载体(AAV) B 型血友病 Zynteglo Bluebird bio Inc. 基因递送-慢病毒载体(LVV) β-地中海贫血 据参考资料内容显示,大约60%的单基因病最终都会导致神经系统症状,截止目前很多引发神经系统疾病的基因突变类型基本得以确认。 而基因载体递送技术,可通过一次给药将治疗基因转入神经元或其他神经细胞中,且具有长期疗效,在中枢神经系统疾病的治疗中有很大的优势,如利用AAV递送到帕金森病患者大脑中的芳香氨基酸脱羧酶就可持续表达4年,而在非人灵长类动物中则可持续表达15年。 药品名称 企业 技术类型 适应症 SKYSONA Bluebird bio, Inc. 基因递送-慢病毒载体(LVV) 活动性脑肾上腺脑白质营养不良 神经肌肉疾病 FDA批准的“神经肌肉罕见病”新药 药品名称 企业 技术类型 适应症 Elevidys Sarepta Therapeutics/罗氏 基因递送-腺病毒载体(AAV) 杜氏肌营养不良症(DMD) ZOLGENSMA Novartis Gene Therapies, Inc 脊髓性肌萎缩症(Ⅰ型) 视网膜及视神经疾病 FDA批准的“视网膜及视神经罕见病”新药 药品名称 企业 技术类型 适应症 LUXTURNA Spark Therapeutics, Inc. 基因递送-腺病毒载体(AAV) 双等位基因 RPE65 突变相关性视网膜营养不良 国内罕见病基因疗法研发火热 与海外相比,我国罕见病基因治疗起步较晚,现阶段罕见病基因疗法管线仅有美国的1/3左右,且多数基因疗法尚处于临床前期,但由于我国较大的患者基数,大量基因疗法基础研究的进步与相关人才爆发,我国罕见病基因治疗的发展速度远高于全球平均水平,截至目前,基因疗法的临床试验数量仅次于美国,增速全球第一。 数据来源:药智数据 近一年国内原研活跃基因疗法(部分) (建议横屏观看)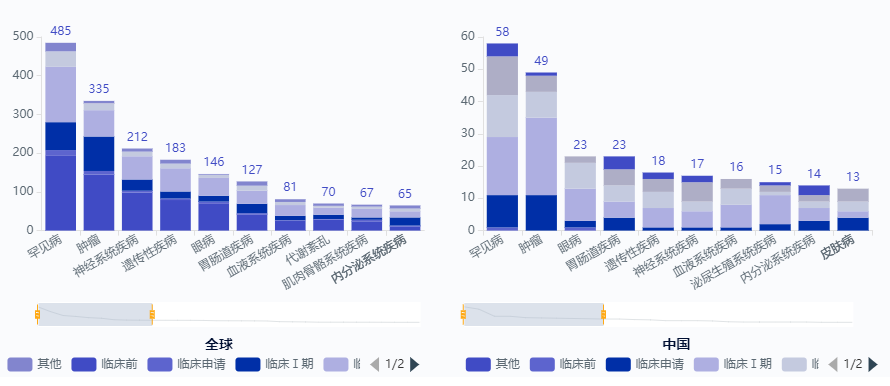


基因治疗作为一种新兴的治疗手段,原则上有望解决所有单基因病的治疗困境,而作为单基因病集中地的罕见病领域则也最有望取得率先突破。 目前来讲,基因递送技术已经被应用于多项罕见遗传病的临床试验,涵盖眼病、血液病、神经系统疾病等多个领域,AAV作为当下最安全、长效的病毒载体,是治疗罕见单基因病最被寄予厚望的平台,有望在未来5—10年里全面爆发。另外,基因编辑技术的应用愈发熟练,技术走向了成熟,也使原有因致病基因过大,超出病毒载体的包装限制而不能运用基因递送方法治疗的疾病得到了突破性进展,首款基因编辑疗法Casgevy获批上市不仅拉开了基因治疗的新序幕,后续TALEN/ZFN/碱基编辑等基因编辑技术也在迅速发展中,前途不可限量。 但是,基因治疗作为一种复杂疗法,要想应用至临床来治疗更多更广泛的遗传性罕见病,尚存在诸多问题亟待解决,如改善整合基因载体和脱靶效应带来的遗传毒性、控制靶基因体内的表达量维持在有效治疗疾病水平、在不降低其活性的基础上延长半衰期、解决伦理问题和高昂的治疗费用等。 在这些方面,全球基因疗法的研发企业和CDMO企业也在积极布局,从研发与技术上、从工艺端,应对工艺难点,降低工艺成本和偏差,如博腾股份旗下的博腾生物,作为细胞与基因治疗CRO+CDMO公司,可以提供基因编辑CRO服务与质粒和AAV相关CDMO服务,已投入运行的10条病毒载体线可完全满足基因治疗产品的临床期与商业生产需要。 前路漫漫亦灿灿,唯愿更多有识之士能共同努力,为更多罕见病患者的基因治疗需求奋斗终生,让更多幻想能成为现实。 宣建伟, 孙巧. 中国罕见病药物经济学评估适用模型与支付阈值参考标准探讨[J]. 国际药学研究杂志, 2019(9). 李玉欢,李伟.罕见病的基因治疗研究进展.《罕少疾病杂志》,2023(3) 桂怡婷,李强 ,桂永浩.罕见病的基因治疗应用与展望.《临床儿科杂志》. 2020(10) 基因疗法在罕见病上的应用, 劲帆生物,2023-03-31 百亿罕见病市场,基因疗法或为破局之道, 同写意, 2023-04-12
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 2 Qiande Road, Life Science High Tech Zone, Jiang Ning District, Nanjing, Jiangsu Province, China