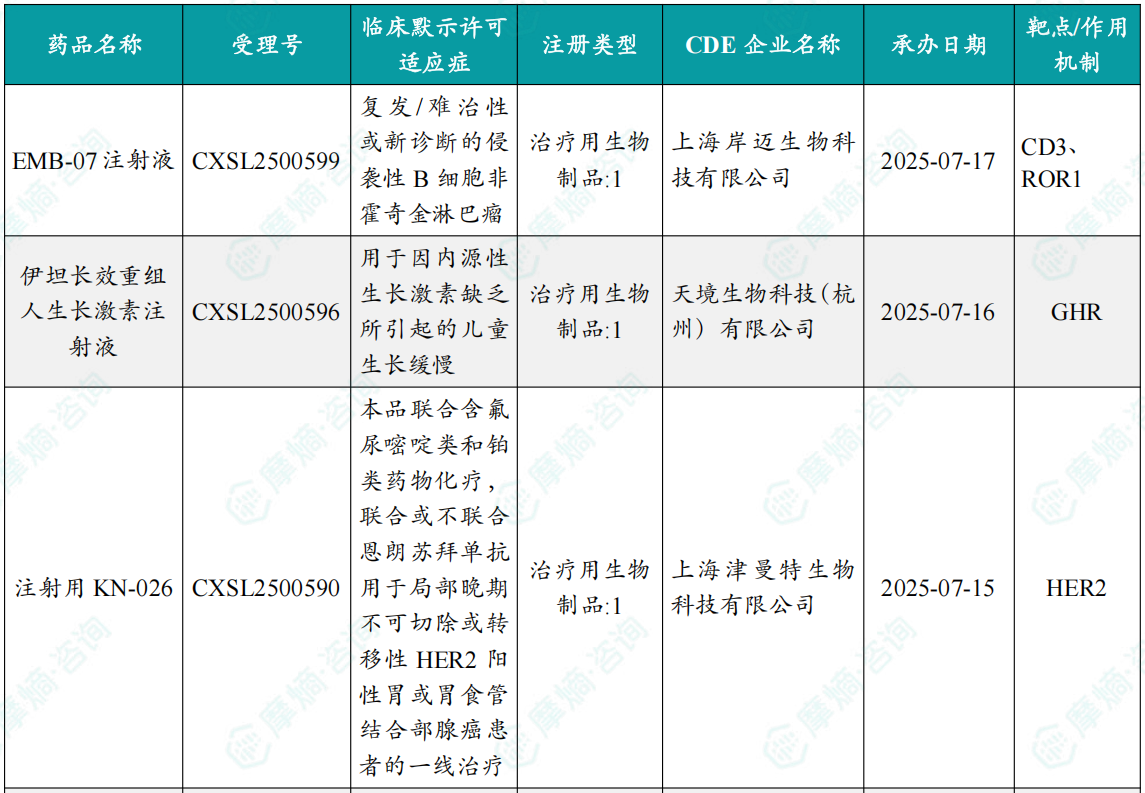
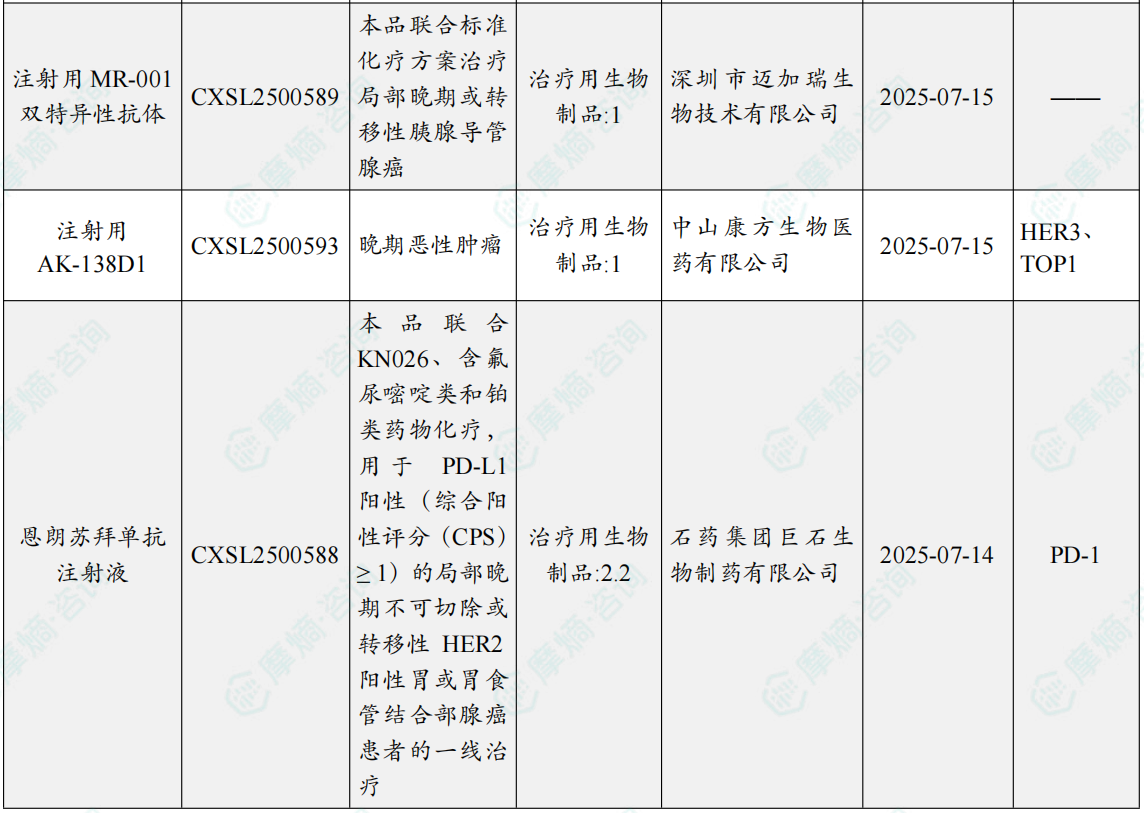
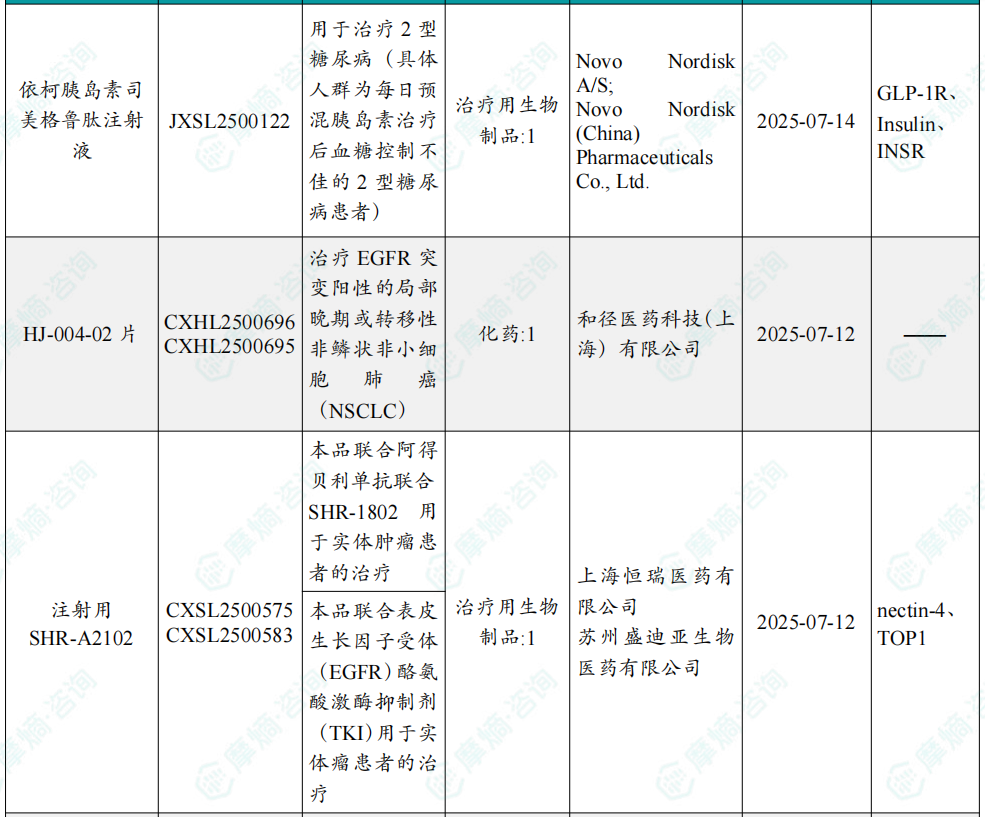
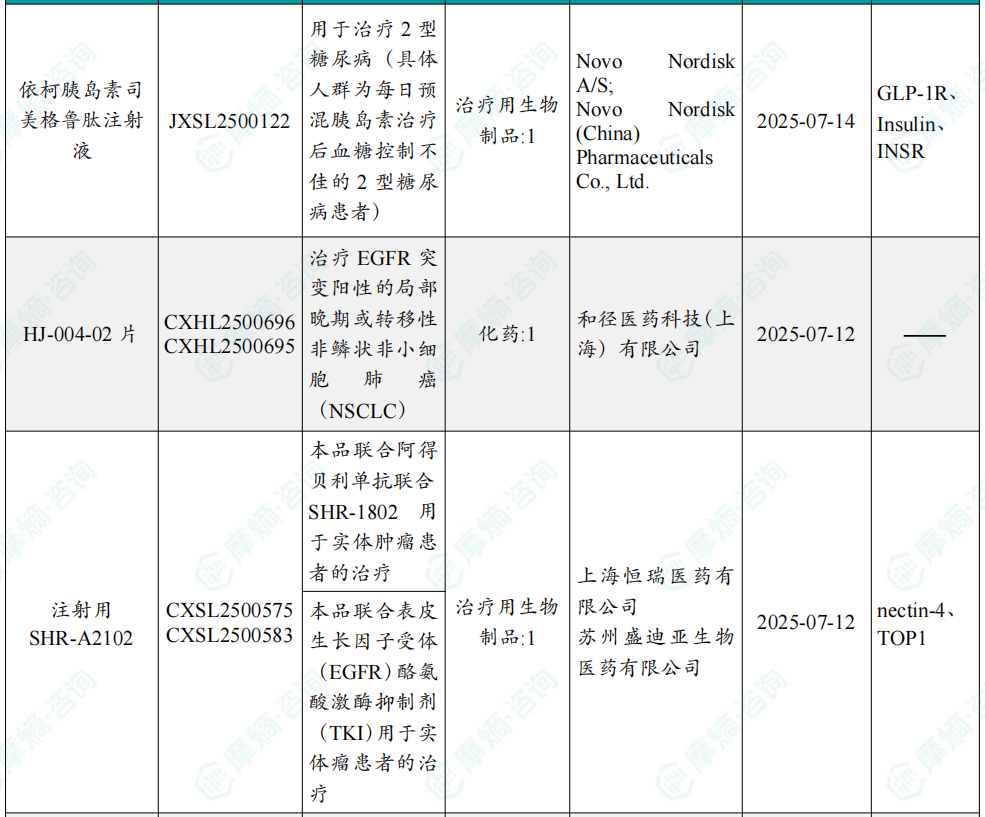
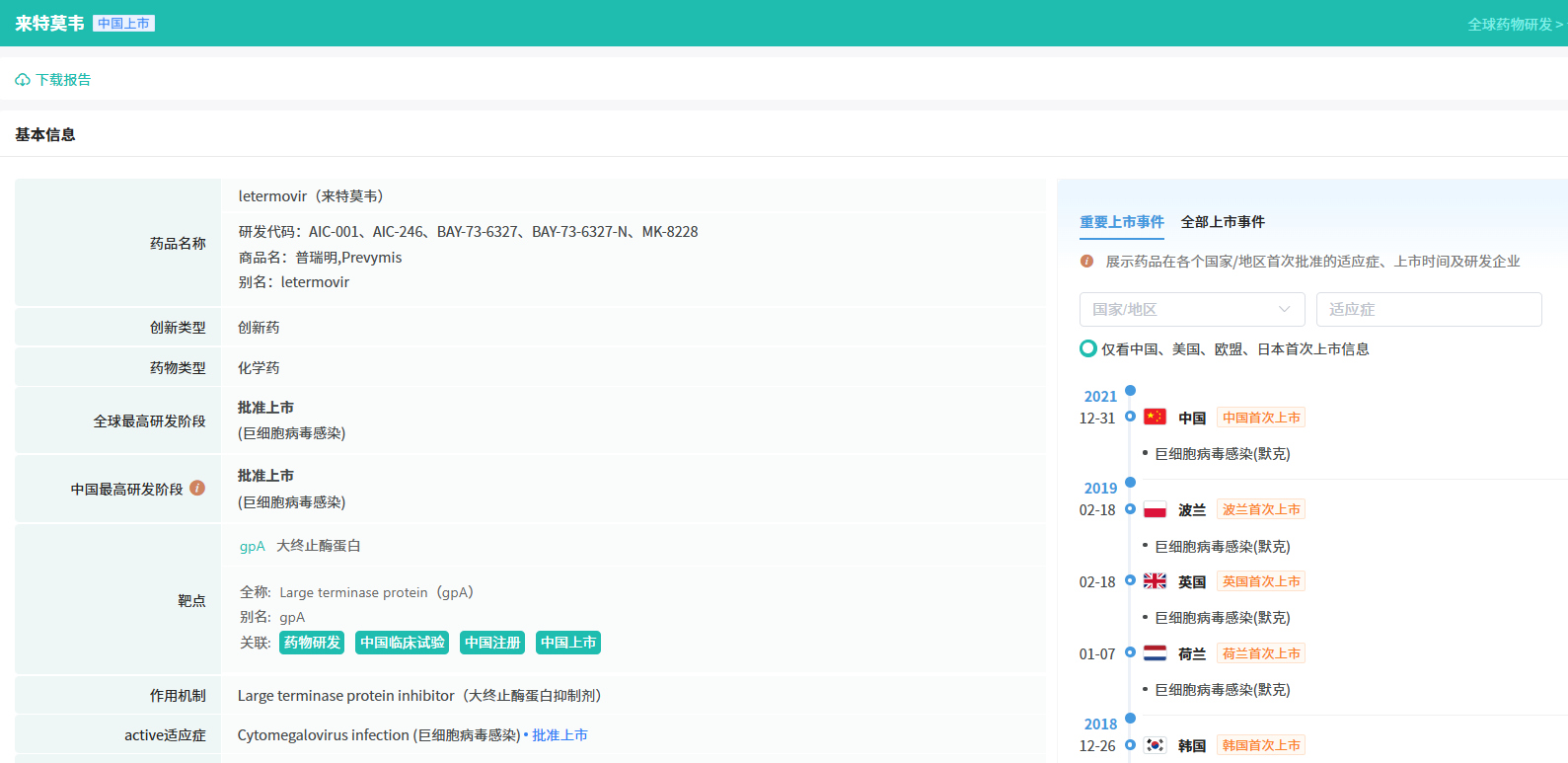
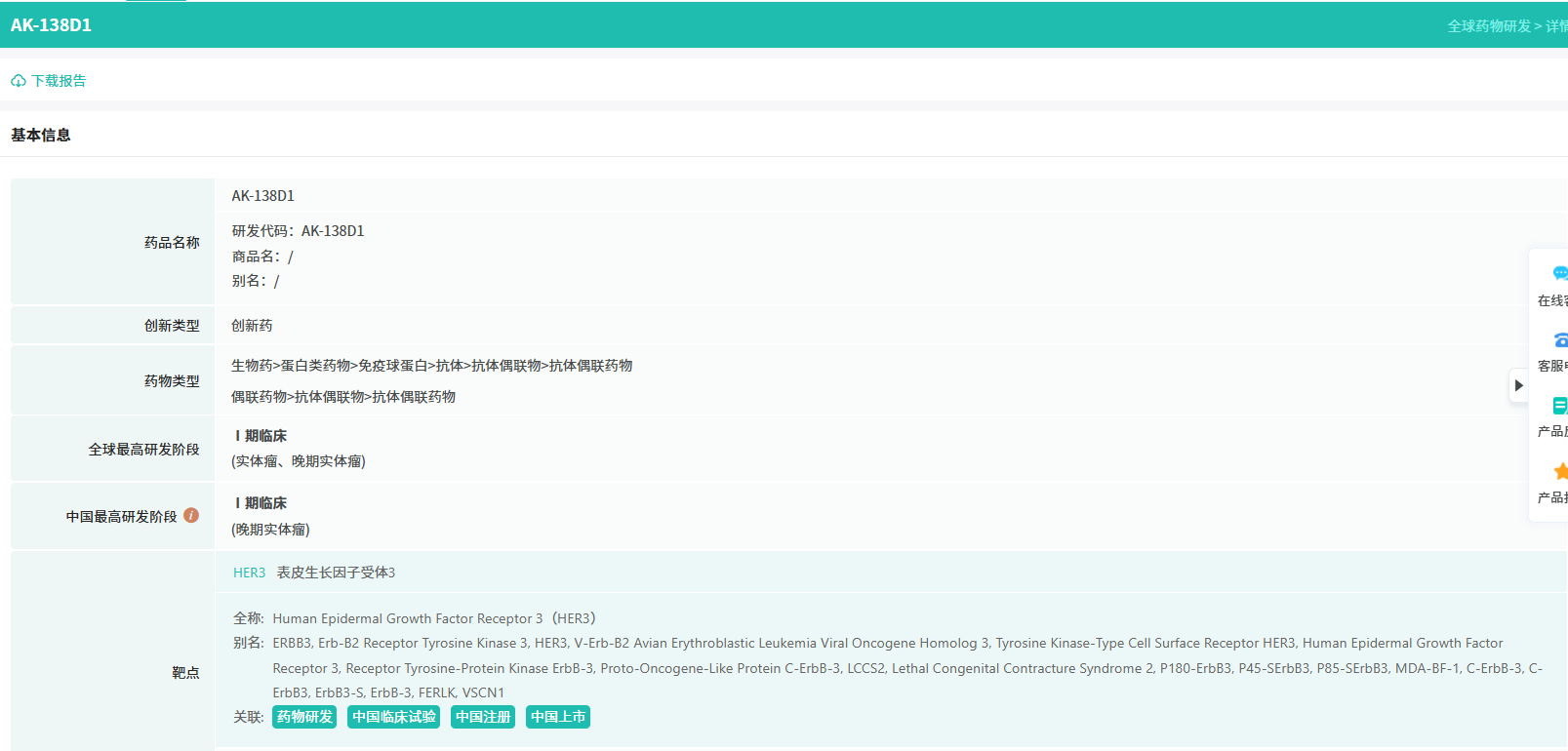
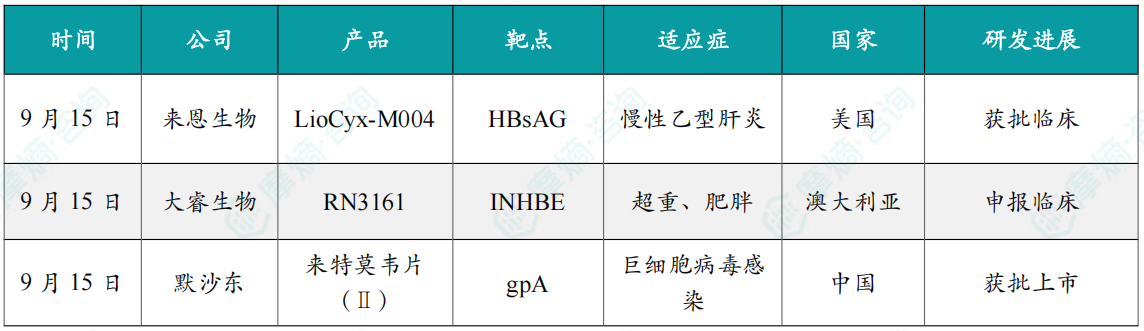
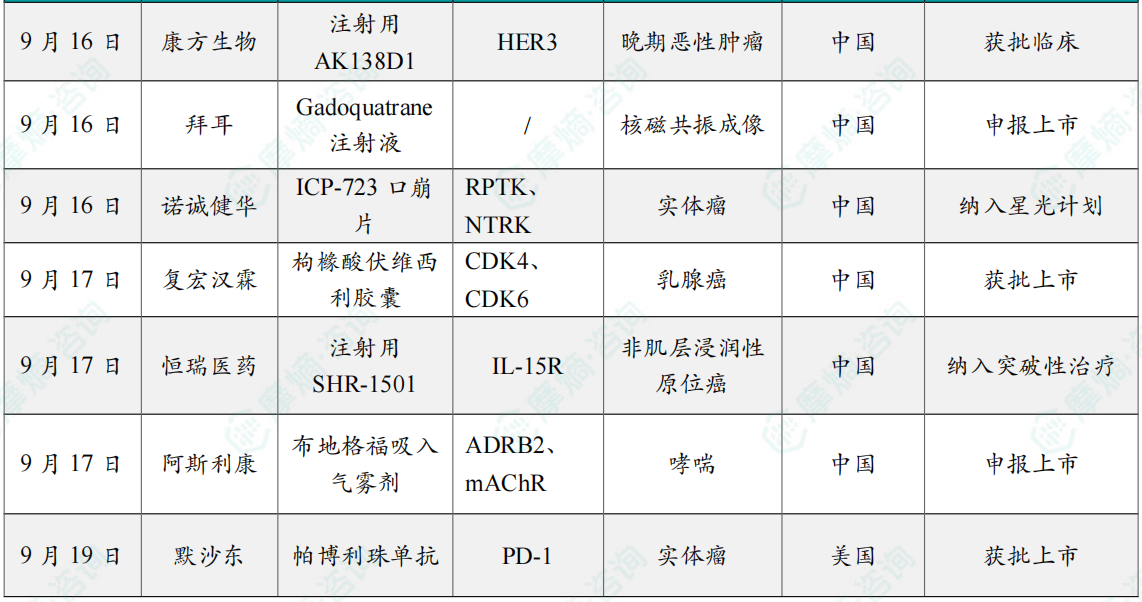
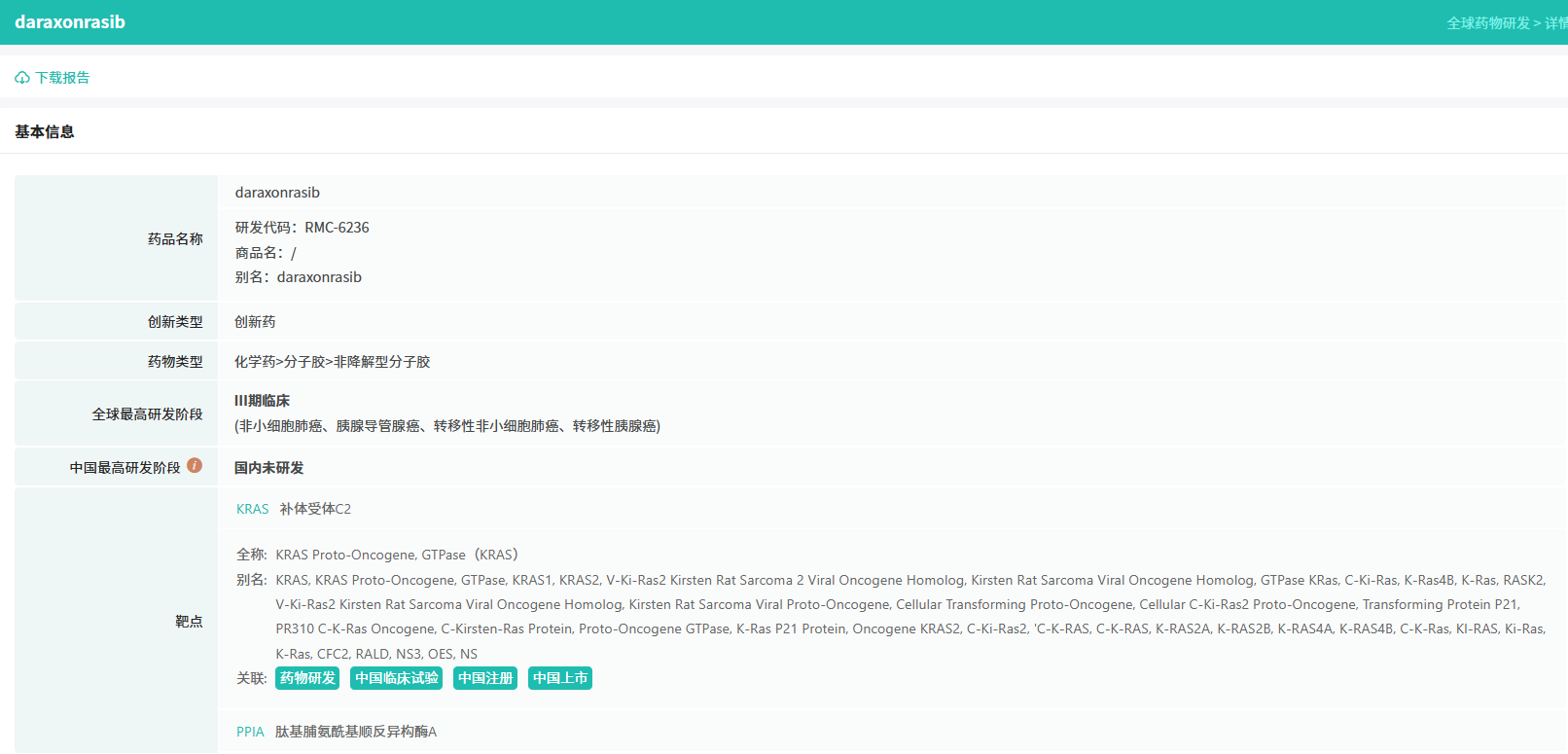
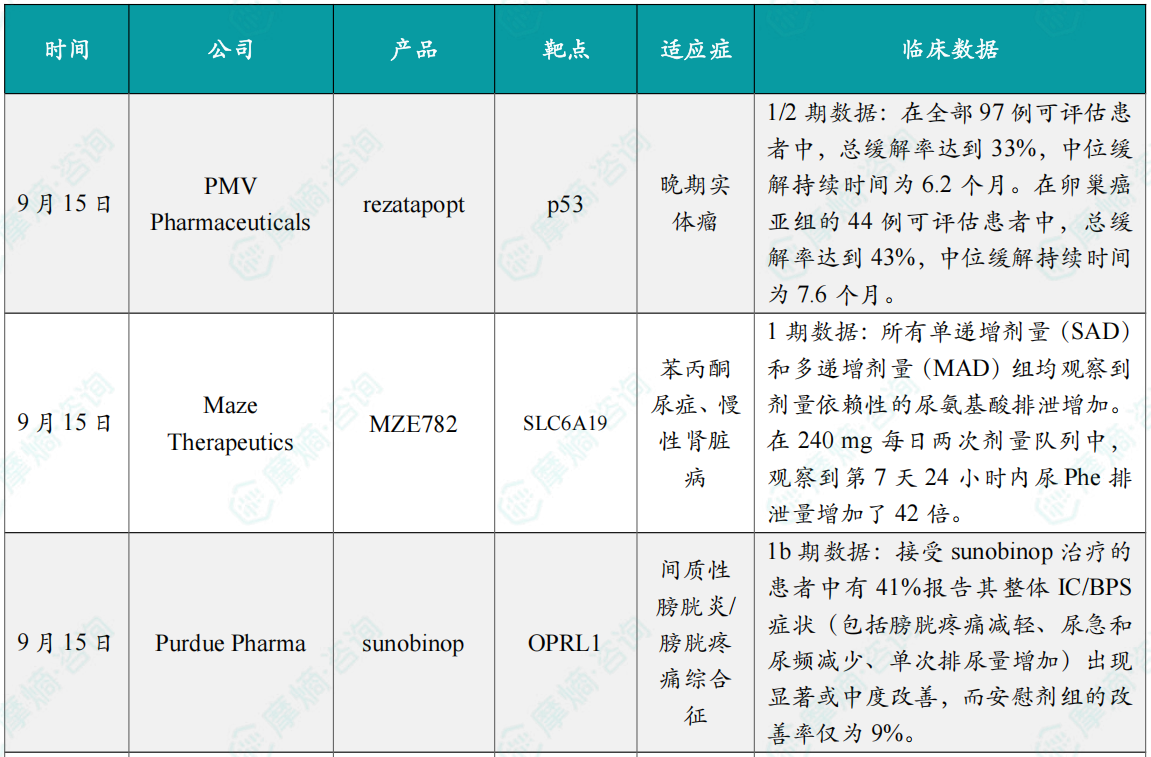
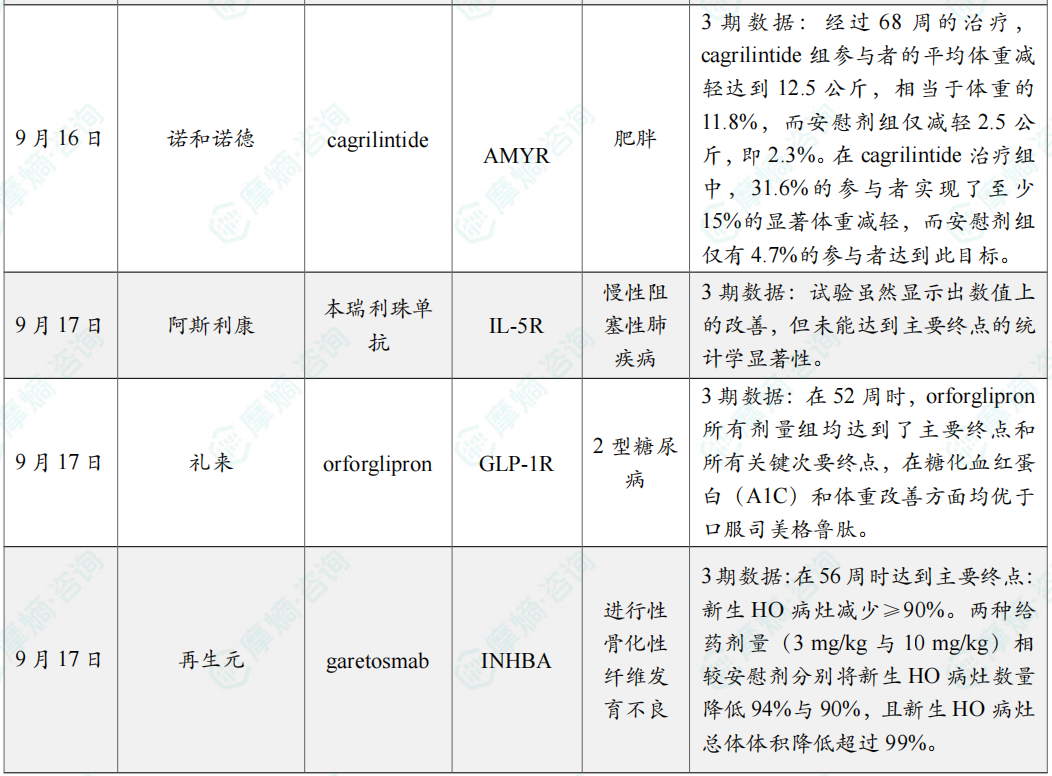
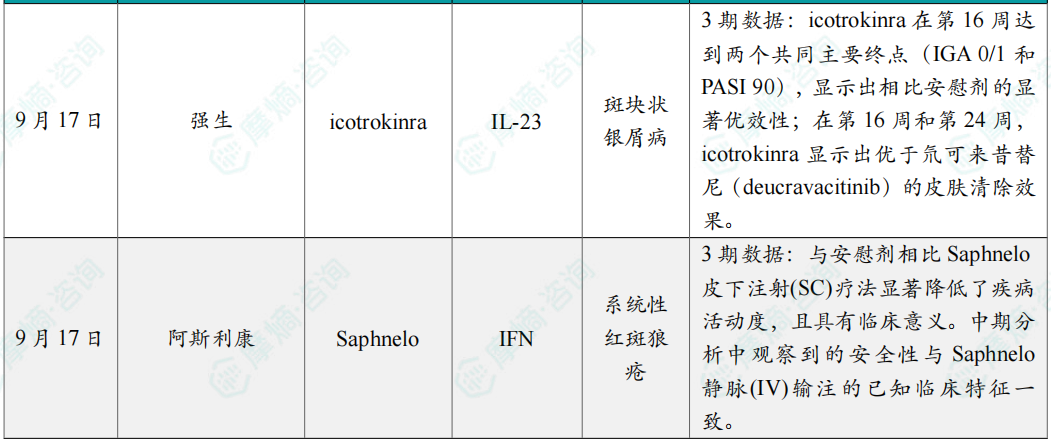
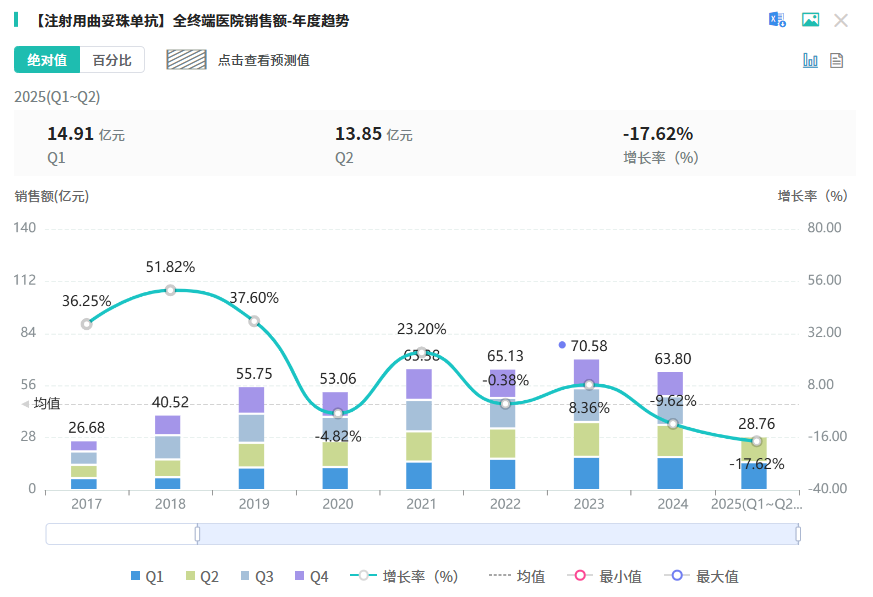
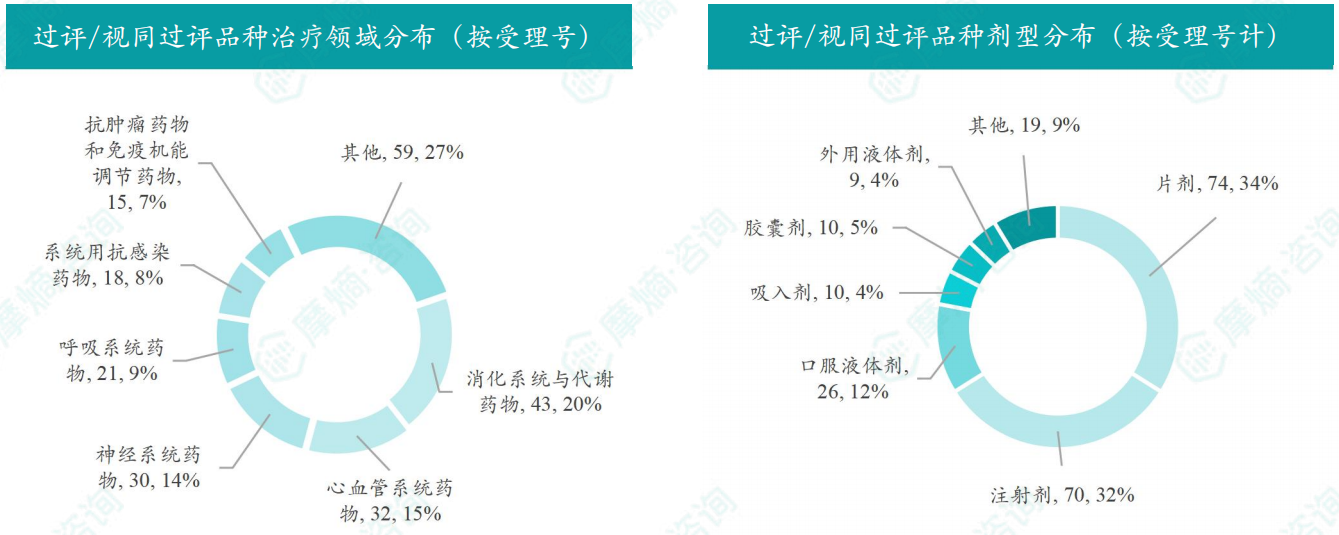
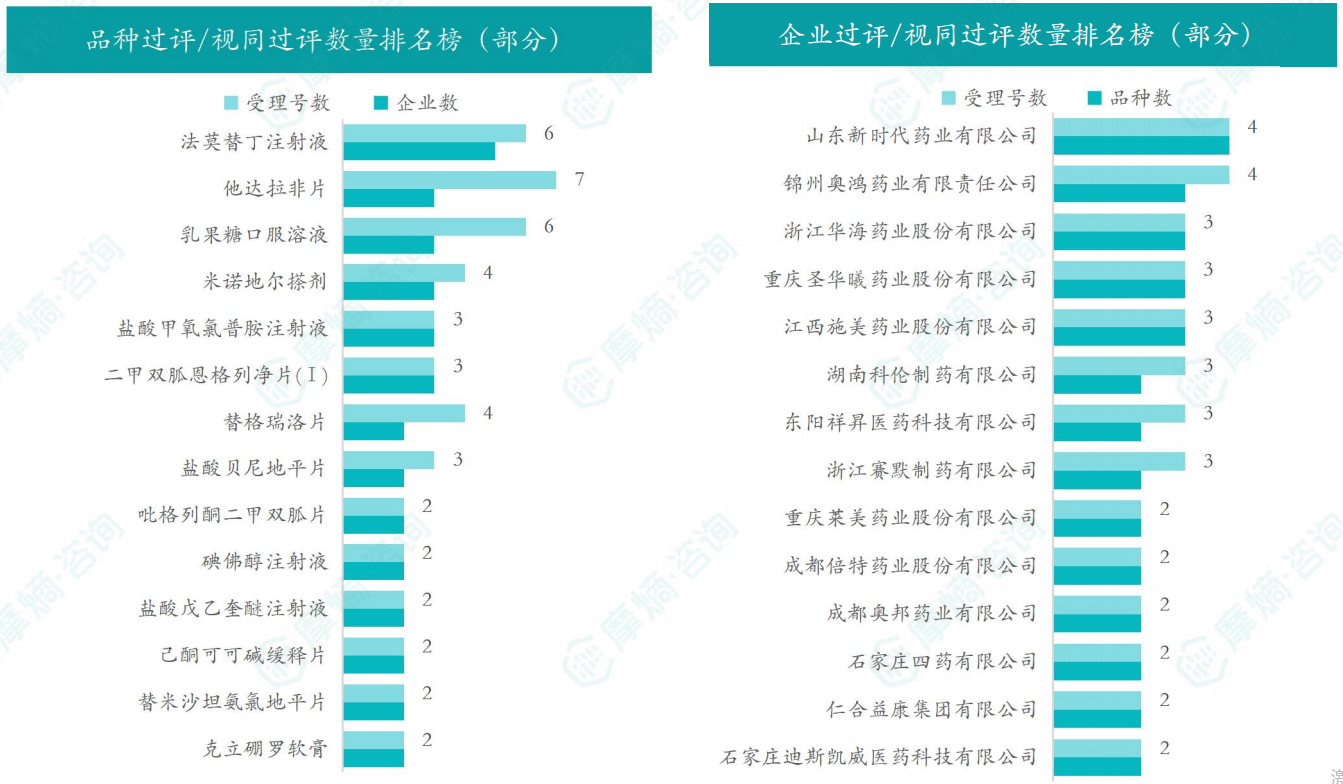
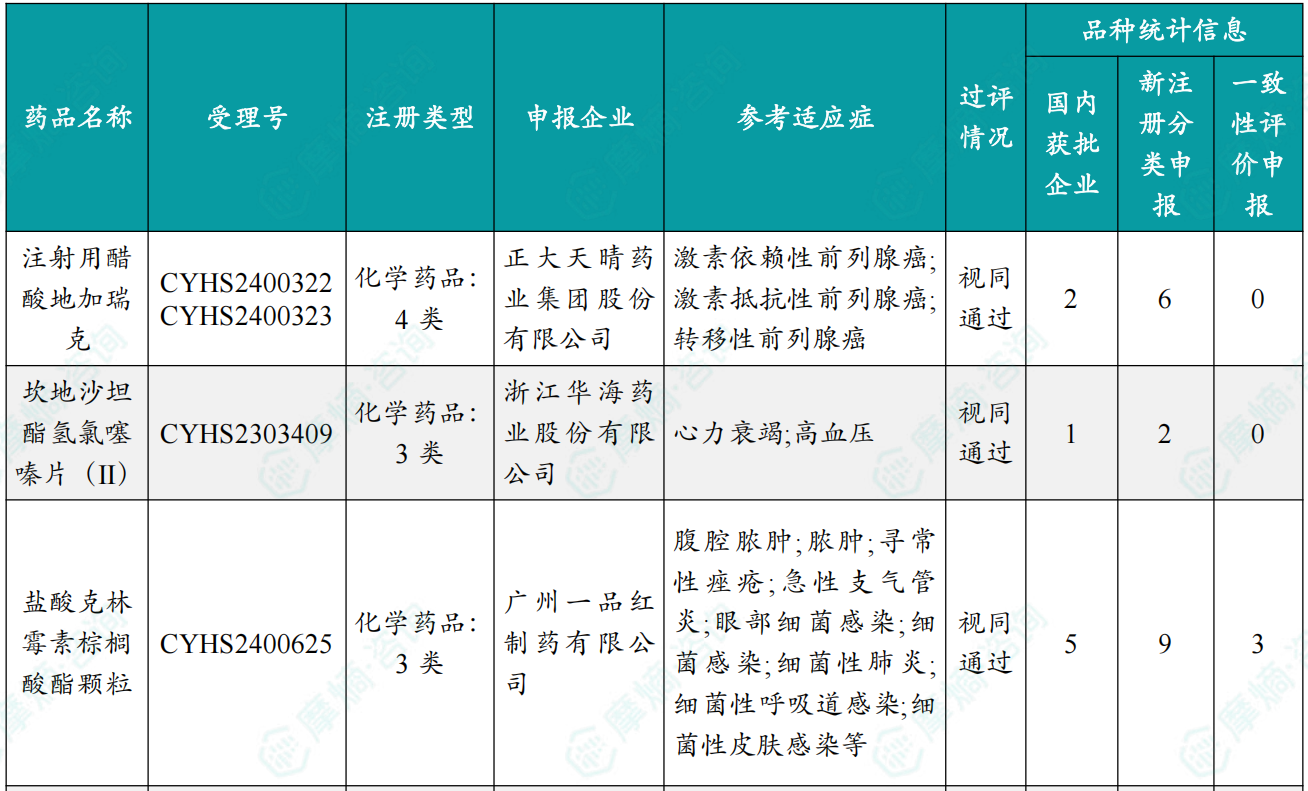
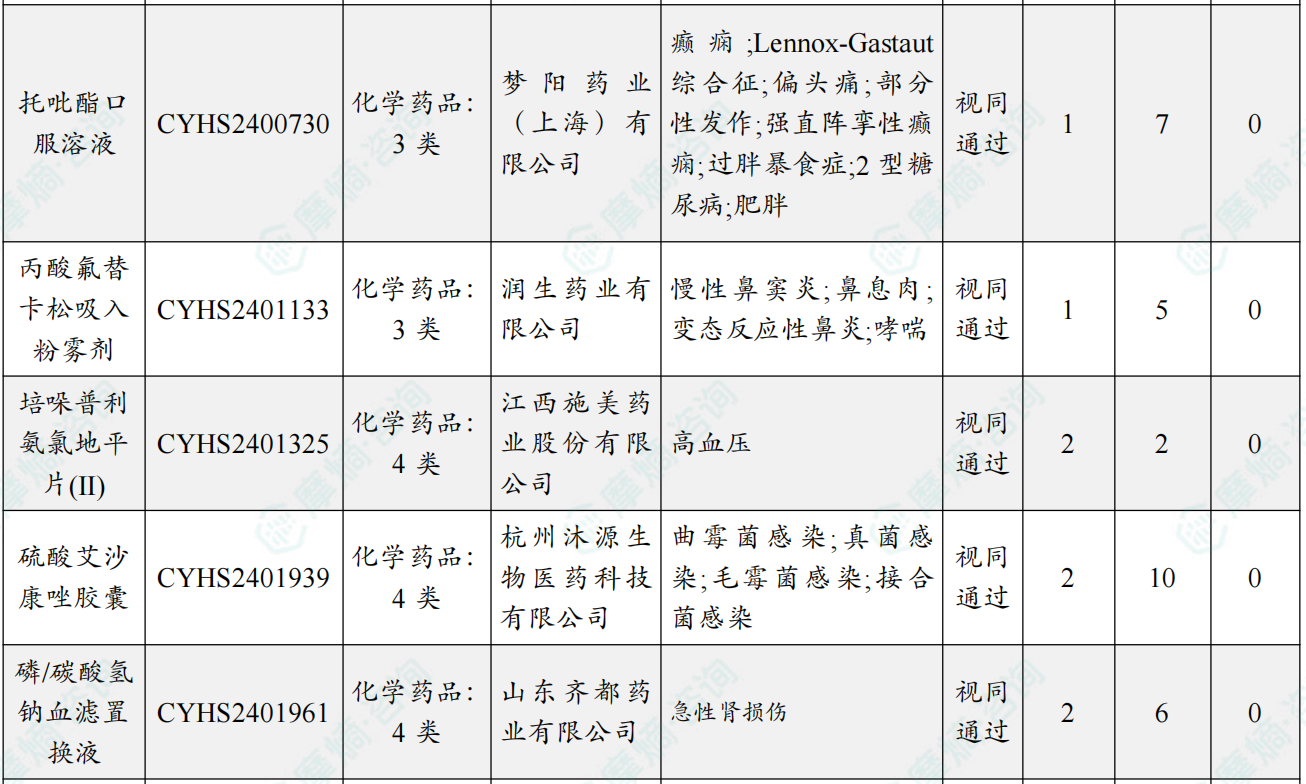
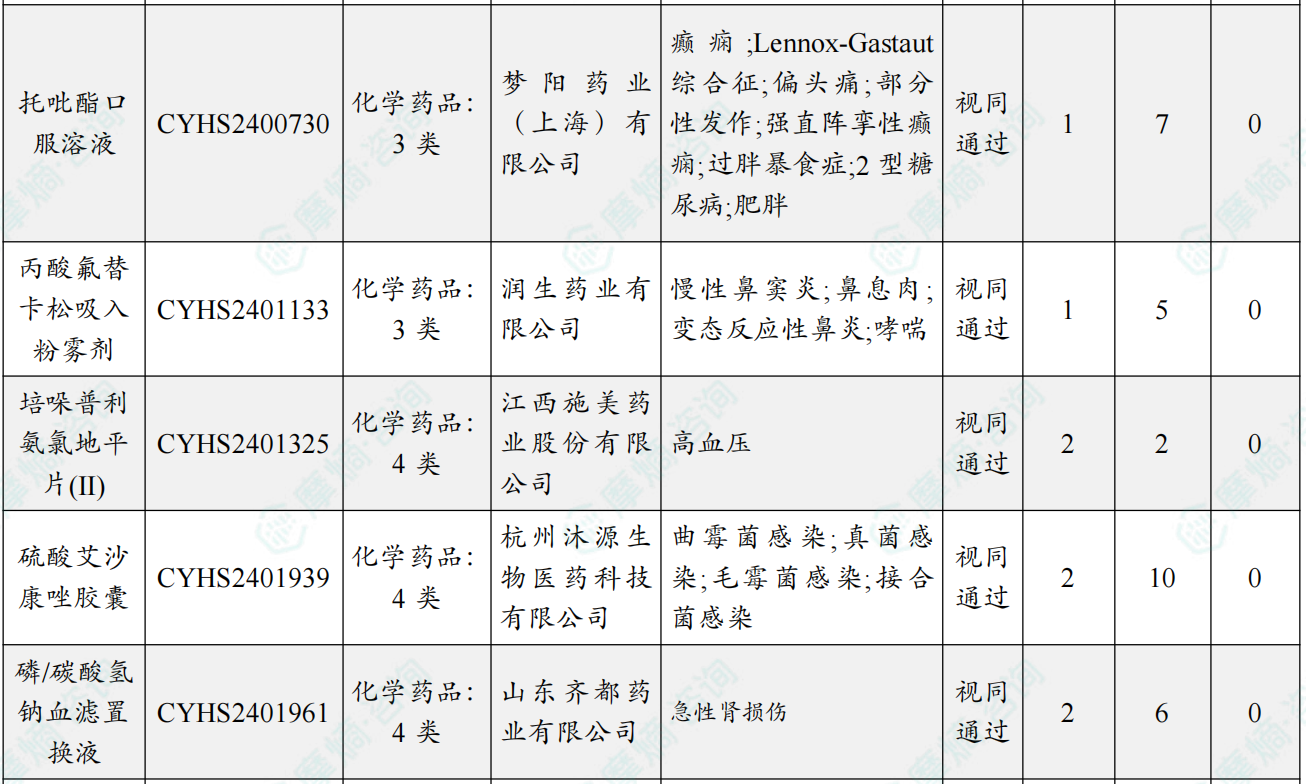
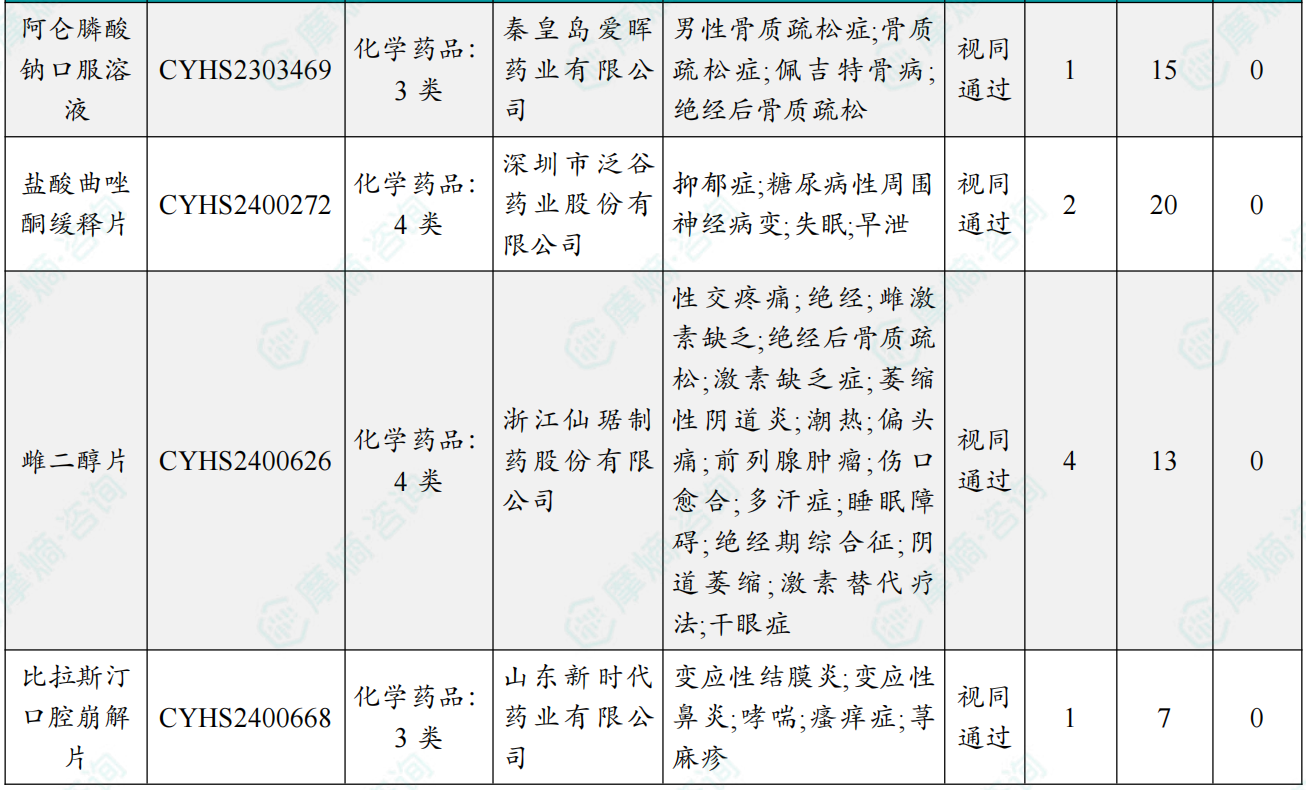
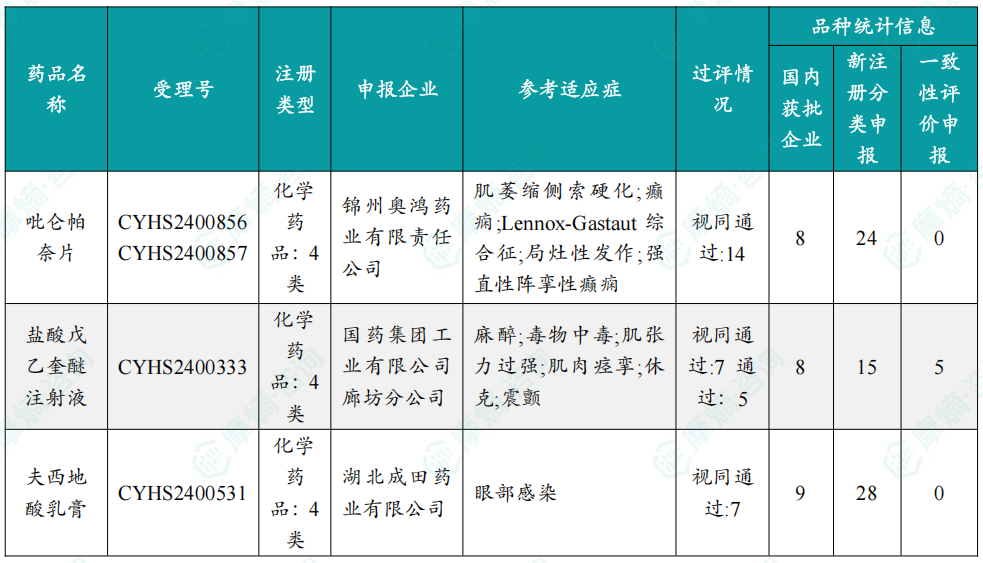
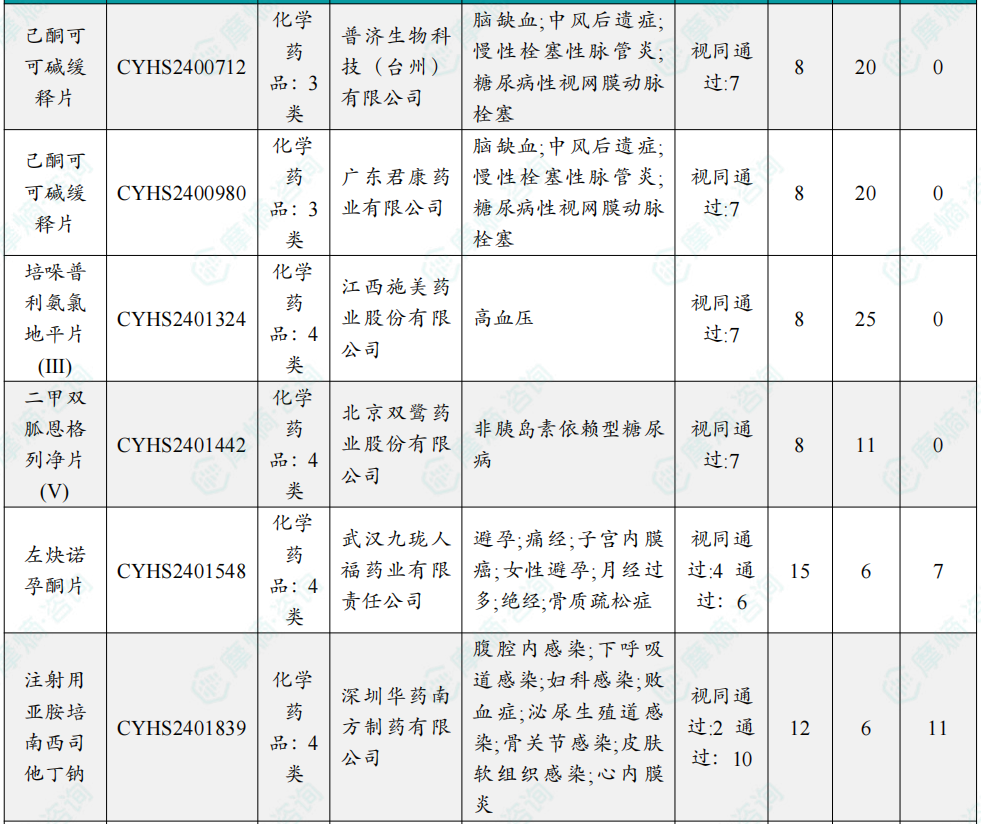
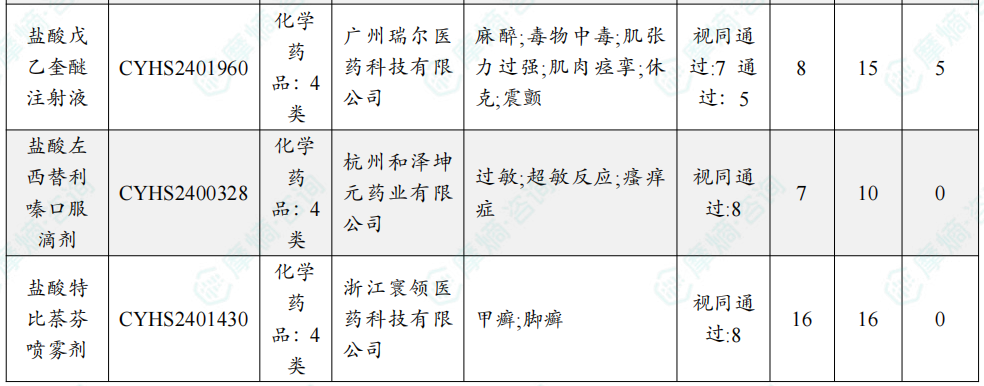
随着全球医药行业的快速发展,新药研发与创新已成为推动行业进步的重要动力。近期,根据摩熵医药数据统计,新药申请与审批获批频繁,显示出医药创新领域的活跃态势。 本文将深入分析2025年9月15日至2025年9月21日期间,国内外新药申请、临床试验批准、仿制药一致性评价等多个方面的最新进展,为用户提供全面的行业资讯。 根据摩熵医药数据库统计,2025年9月15日至9月21日期间,共有61个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号36个,进口药品受理号25个。 本周共计66款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药28款,生物药35款,中药3款。 注:完整数据可识别“文末”二维码下载查看 9月15日,默沙东宣布其新型非核苷类巨细胞病毒(CMV)抑制剂来特莫韦(商品名:普瑞明)的全新剂型——来特莫韦片(Ⅱ)在中国获批上市,用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人和 6 个月及以上且体重≥6kg 的儿童受者[R+]预防巨细胞病毒感染和巨细胞病毒病。 截图来源:摩熵医药全球药物研发数据库 来特莫韦是国内首个且目前唯一可用于接受 HSCT 成人和儿童患者的 CMV 预防方案。来特莫韦片(Ⅱ)包含20mg/袋和 120mg/袋两种规格,满足了来特莫韦适应症内覆盖的各年龄和体重患者的剂量需求,此前,来特莫韦已在中国获批来特莫韦片与来特莫韦注射液两种剂型。 此外,9月16日,CDE官网公示,康方生物申报的1类新药注射用 AK138D1 获批临床试验默示许可,拟开发治疗晚期恶性肿瘤。 截图来源:摩熵医药全球药物研发数据库 公开资料显示,这是康方生物研发的差异化靶向人表皮生长因子受体 3(HER3)的抗体偶联药物(ADC),也是该公司首个进入临床阶段的ADC药物。今年2月,该产品治疗晚期恶性肿瘤的1期临床研究在澳洲完成首例受试者入组。 本周全球 TOP10 创新药研发进展 截图来源:摩熵医药周报 本周全球多项临床试验结果亮点纷呈。9月15日,Revolution Medicines 公司宣布了其 RAS(ON)多重选择性抑制daraxonrasib(RMC-6236)的 1 期临床试验的最新进展。Daraxonrasib是一款口服选择性抑制剂,能够靶向处于GTP结合(激活、ON)状态的突变型及野生型 RAS 蛋白。 截图来源:摩熵医药全球药物研发数据库 该疗法曾在 2025年6月获美国 FDA 授予突破性疗法认定,用于治疗既往接受治疗、携带 KRAS G12 突变的转移性胰腺导管腺癌(PDAC)患者。 9月17日,阿斯利康宣布,其Fasenra(本瑞利珠单抗)治疗慢性阻塞性肺疾病(COPD)的III期RESOLUTE试验虽然显示出数值上的改善,但未能达到主要终点的统计学显著性。该试验中本瑞利珠单抗的安全性与耐受性特征与已知特性一致。 本周全球 TOP10 积极/失败临床结果 截图来源:摩熵医药周报 根据摩熵医药数据库统计,9月15日至9月21日期间,共有88项仿制药申报上市/申报临床获CDE承办,其中新注册分类上市申请受理号79项(包括化药3类,4类),新注册分类临床申请受理号8项(包括化药3类8),一致性评价申请1项。本周10个品种通过一致性评价(按受理号计14项),本周132个品种视同通过一致性评价(按受理号计204项)。本周有6项生物类似物注册申报动态,成都景泽生物制药的重组人促卵泡激素注射液(2项)、安徽安科生物工程(集团)的注射用曲妥珠单抗、迈威(上海)生物的阿柏西普眼内注射溶液、宜昌东阳光长江药业的精蛋白重组人胰岛素混合注射液(30R)和上海生物制品的利妥昔单抗注射液。其中注射用曲妥珠单抗在2024年全终端医院销售额超60亿元。 截图来源:摩熵医药全终端医院销售数据库 本周过评/视同过评品种主要为消化系统与代谢药物;过评/视同过评产品剂型主要为片剂;本周他达拉非片品种过评/视同过评受理号数量最多达7个。 截图来源:摩熵医药周报 本周法莫替丁注射液品种过评/视同过评企业最多达5家;本周山东新时代药业有限公司过评/视同过评品种数最多达4种,本周过评/视同过评企业共包括浙江华海药业股份有限公司、湖南科伦制药有限公司和石家庄四药有限公司等153家企业。 截图来源:摩熵医药周报 本周有注射用醋酸地加瑞克、坎地沙坦酯氢氯噻嗪片(Ⅱ)、盐酸克林霉素棕榈酸酯颗粒等13款首次过评/视同过评品种。 本周首次过评/视同过评品种 截图来源:摩熵医药周报 此外,吡仑帕奈片、盐酸戊乙奎醚注射液、夫西地酸乳膏等10款过评/视同过评达7家企业品种。 截图来源:摩熵医药周报
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 2 Qiande Road, Life Science High Tech Zone, Jiang Ning District, Nanjing, Jiangsu Province, China