多发性骨髓瘤(MM)是一种克隆浆细胞异常增殖的恶性血液肿瘤,好发于中老年人群,以骨痛、贫血、肾功能损害和高钙血症为主要临床表现。作为全球第二常见的血液系统恶性肿瘤,其治疗策略的每一次革新都牵动着无数患者的希望。2026年1月6日,美国临床肿瘤学会(ASCO)与安大略省健康/癌症护理安大略(OH-CCO)联合发布了《多发性骨髓瘤治疗:ASCO-Ontario Health动态指南》,这是继2019年版后的重大更新。本次更新被定义为“动态指南”(Living Guideline),意味着专家组将持续系统地审查最新医学文献,根据新证据定期更新推荐,而非传统意义上每隔数年才修订一次。这一机制创新,正是为了适应骨髓瘤治疗领域日新月异的节奏。从2019到2026年,短短七年间,骨髓瘤治疗格局发生了翻天覆地的变化:CAR-T细胞疗法和双特异性抗体等免疫治疗横空出世,四药联合方案成为新诊断患者的标准选择,冒烟型骨髓瘤的治疗介入时机重新界定。本文将基于161项随机对照试验(RCT)的证据基础,深入解读这份指南的核心变革与临床意义。
一、指南更新的四大驱动力
1.1上一版指南的局限性
2019年版指南发布后,骨髓瘤治疗领域经历了爆发式的发展。原有建议已无法满足临床需求,主要体现在三个方面:指南滞后于临床实践、缺乏针对新药的指导、冒烟型骨髓瘤(SMM)定义陈旧。当时被视为前沿的三药方案,如今已成为基础治疗;而CAR-T、双抗等革命性疗法更是尚未进入主流视野。
1.2新疗法的涌现
数年来,大量高质量RCT相继发表,特别是CAR-T细胞疗法(如Ide-cel、Cilta-cel)和双特异性抗体(如Teclistamab、Elranatamab等)的问世,彻底改变了复发/难治性骨髓瘤的治疗范式。这些免疫治疗不仅带来了前所未有的深度缓解率,更重塑了我们对"治愈"可能性的认知。
1.3疗效的显著提升
新药组合方案显著改善了患者的无进展生存期(PFS)。以新诊断适合移植患者为例,从早期的双药化疗,到三药联合,再到如今的四药方案,中位PFS已从2-3年延长至5年以上,部分患者甚至有望实现功能性治愈。
1.4定义的变更
2014年国际骨髓瘤工作组(IMWG)更新的SLiM CRAB标准,将部分超高危SMM重新划分为活动性MM,改变了SMM的人群构成。这一诊断标准的演进,使得"何时启动治疗"这一经典命题需要重新审视。 图2. 最新指南的数据规模——基于161项RCT的证据基础
图2. 最新指南的数据规模——基于161项RCT的证据基础
二、冒烟型骨髓瘤:从“观察等待“到”选择性干预“
2.1 SMM的定义与自然病程
冒烟型骨髓瘤(Smoldering Multiple Myeloma, SMM)是介于意义未明的单克隆丙种球蛋白病(MGUS)与活动性MM之间的无症状浆细胞疾病。其本质并非静态的疾病状态,而是对未来进展可能性的"统计学评估"。传统数据显示,SMM患者面临10%/年的进展风险(前5年),随后降至3%/年(5-10年)和1%/年(>10年)。即使经过20年随访,仍有20%的个体未发展为活动性MM。这一自然病程的异质性,构成了治疗决策的核心挑战。
2.2指南的核心推荐
推荐1.1(条件性推荐):高危SMM患者可选择达雷妥尤单抗(Daratumumab,最长36个月)或积极监测;来那度胺(Lenalidomide)不推荐常规使用。这一推荐基于三项关键RCT:ECOG E3A06(来那度胺vs观察)、QuiRedex(来那度胺+地塞米松vs观察)和AQUILA(达雷妥尤单抗vs积极监测)。值得注意的是,AQUILA研究采用的高危定义包括:骨髓克隆浆细胞≥10%且满足以下至少一项——血清M蛋白≥3g/dL、IgA型SMM、免疫麻痹(两种未受累免疫球蛋白同种型降低)、血清游离轻链比值8-100、骨髓克隆浆细胞比例50%-60%。推荐1.2(强推荐):非高危SMM患者不推荐治疗。推荐1.3(良好实践声明):必须使用当前诊断算法排除活动性MM。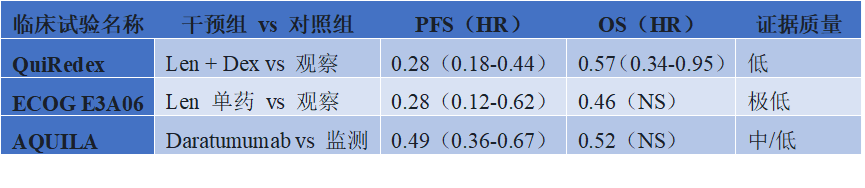 图3. 关键随机对照试验(RCT)的研究结果和证据质量
图3. 关键随机对照试验(RCT)的研究结果和证据质量
2.3临床解读与争议
指南制定过程中,专家组面临的核心争议在于:无症状患者是否应接受系统性抗肿瘤治疗?如果治疗,基于何种标准?推荐何种方案?指导原则遵循“首先不伤害“(Primum non nocere)——对于无症状患者,启动长期有毒性治疗的门槛必须显著高于活动性MM患者。专家组认为,达雷妥尤单抗的潜在PFS和OS获益可能超过其增加的毒性,故作为积极监测的替代选择;而来那度胺因证据不确定性较高,未获常规推荐。需要强调的是,SMM风险模型尚未统一(PETHEMA、Mayo 2018、IMWG、PANGEA等模型的一致性仅16.6%),且三项关键试验采用的高危定义各异,导致证据的间接性。临床实践中,需结合个体因素谨慎评估。
三、新诊断适合移植患者:四药诱导+移植+维持的标准模式
3.1 诱导治疗:四药方案成为首选
推荐2.2.1(强推荐):适合移植患者应接受4个月诱导治疗,方案为达雷妥尤单抗或艾沙妥珠单抗(Isatuximab)联合硼替佐米、来那度胺和地塞米松(Dara/Isa-VRd)。这一推荐的证据基础来自PERSEUS、GRIFFIN和GMMG-HD7三项关键试验。这些研究一致显示,在VRd基础上加用CD38单抗可显著改善PFS,且未显著增加不可接受的毒性。在来那度胺可及性受限的地区,可用沙利度胺替代(CASSIOPEIA试验支持Dara-VTd方案)。推荐2.2.3(条件性推荐):如毒性担忧,可用卡非佐米(Carfilzomib)替代硼替佐米。图4. 新诊断MM(NDMM)适合移植及不适合移植患者的诱导治疗方案
3.2 干细胞移植:地位稳固但时机灵活
推荐2.3.1(强推荐):所有适合移植患者应接受 upfront ASCT(前期自体干细胞移植)。DETERMINATION试验的长期随访(中位76个月)证实,延迟ASCT与较差的PFS相关(HR=1.53),尽管OS无显著差异。值得注意的是,仅35%的非移植组患者后续接受了ASCT,提示“延迟“可能演变为“错过“。推荐2.3.3(良好实践声明):无论移植意向如何,诱导治疗4-6个月内应采集足够干细胞(至少支持两次ASCT),以备后续治疗之需。
3.3 巩固与维持治疗
推荐2.2.2(条件性推荐):对于接受Dara-VRd诱导且计划移植后巩固的患者,可给予2周期Dara-VRd巩固。推荐2.4.1(强推荐):应给予来那度胺维持治疗,至少2年。推荐2.4.2(条件性推荐):可在此基础上加用卡非佐米或达雷妥尤单抗(±地塞米松),尤其适用于高危细胞遗传学异常患者。维持治疗的持续时间仍是未解之谜。GMMG-MM5试验比较了2年固定疗程与持续治疗至进展,未发现PFS差异,但非劣效设计限制了结论的外推。当前实践建议:至少2年来那度胺,后续决策基于患者偏好、缓解深度和持续时间,以及毒性-获益权衡。
四、新诊断不适合移植患者:个体化四药或三药方案
4.1 治疗策略的分层
不适合移植患者的治疗需综合考虑年龄、合并症、虚弱状态(frailty)和患者意愿。指南构建了清晰的分层框架:适合强力治疗者:四药方案(Dara/Isa-VRd)虚弱/不适合强力治疗者:三药方案(Dara-Rd或VRd)
4.2 核心推荐
推荐3.1.1(强推荐):非虚弱、可耐受治疗的不适合移植患者,应接受CD38单抗(达雷妥尤单抗或艾沙妥珠单抗)联合硼替佐米、来那度胺和地塞米松。IMROZ和CEPHEUS两项关键试验确立了四药方案在该人群中的地位。IMROZ研究显示Isa-VRd显著改善PFS;CEPHEUS研究证实Dara-VRd的获益。IFM 2020-05/BENEFIT试验进一步表明,在此类患者中加入硼替佐米可显著提高MRD阴性率。推荐3.1.2(条件性推荐):不适合四药治疗的患者,Dara-Rd或VRd是合理替代。
4.3 实践要点
现代实践中,硼替佐米应采用每周一次给药(而非传统每周两次),以降低周围神经病变发生率而不影响疗效。地塞米松可考虑在6-9个月后减量或停用,以减少长期毒性(如白内障、骨密度下降)。对于80岁以上或IMWG定义虚弱的患者,可参考REST研究的设计:四药方案中地塞米松使用2个月后停用,仍可获得较高的相对剂量强度和MRD阴性率。
五、复发/难治性骨髓瘤:免疫治疗时代的治疗序列
5.1 治疗原则的革新
复发/难治性骨髓瘤(RRMM)的治疗决策是本次指南重构最为彻底的部分。专家组放弃了具体药物的排序推荐,转而提出一系列指导原则:推荐4.3(强推荐):应向符合条件的患者提供三药治疗或T细胞重定向治疗(CAR-T或双特异性抗体)。Ø类别转换(Class Switching):尽可能使用与既往治疗机制不同的药物Ø免疫治疗前移:CAR-T与双特异性抗体应尽早纳入考虑Ø个体化决策:基于毒性耐受性、给药便利性和患者偏好选择方案
5.2 首次复发的策略
对于既往未使用CD38单抗的患者,含CD38单抗的三药方案是合理选择。对于CD38单抗难治者,应转换至含卡非佐米或泊马度胺(Pomalidomide)的方案。此外,KarMMa-3和CARTITUDE-4两项pivotal临床试验确立了CAR-T在2-4线治疗中的地位。CARTITUDE-4更是显示,在来那度胺难治、1-3线治疗后复发的人群中,Cilta-cel较标准三药方案显著改善PFS和OS。
5.3 后续复发与T细胞重定向治疗
对于后续复发,T细胞重定向治疗(CAR-T或双特异性抗体)成为关键选择。专家组强调:ØCAR-T可能不适合快速进展的复发,因其制备需3-6周Ø双特异性抗体(Teclistamab、Elranatamab、Linvoseltamab、Talquetamab)为老年和虚弱患者提供了重要选择Ø最佳治疗序列尚无定论,需基于患者因素、疾病特征、作用机制和既往治疗反应综合决策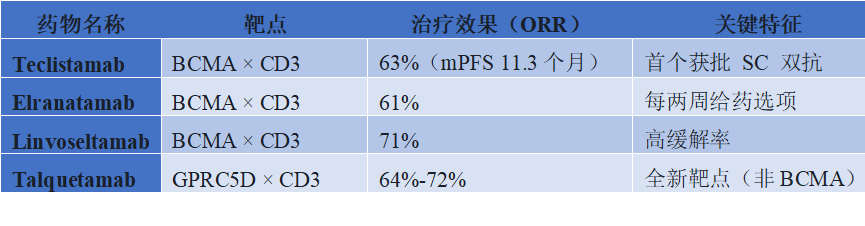 图5. 双特异性抗体关键特征及治疗效果
图5. 双特异性抗体关键特征及治疗效果
5.4 四线及以上复发
对于四线及以上复发,四种药物获得美国FDA批准:三种BCMA×CD3双抗(Elranatamab、Linvoseltamab、Teclistamab)和一种GPRC5D×CD3双抗(Talquetamab)。这些药物在 heavily pretreated 人群中显示出令人鼓舞的疗效,但缺乏直接比较,无法推荐优先顺序。
六、指南的局限性与未来方向
6.1 当前局限
尽管本次更新基于161项RCT的庞大证据基础,仍存在若干未解难题:SMM风险模型不统一导致临床试验入组标准不一致,影响证据的普适性;最佳药物序列(Sequencing)无定论,特别是免疫治疗后的再治疗策略;维持治疗持续时间缺乏随机证据支持基于MRD状态的治疗调整。
6.2 未来研究方向
未来研究方向包括MRD驱动治疗,DRAMMATIC等试验正在探索根据微小残留病灶(MRD)状态决定停药或强化治疗的策略,初步数据显示MRD阴性患者早期停药后3年PFS率可达85%以上,提示维持治疗可能无需无限期持续;老药新用与组合,探索不同机制药物的最佳搭配,如卡非佐米-来那度胺-地塞米松(KRd)±达雷妥尤单抗的ADVANCE试验,以及Isatuximab联合KRd的ISKIA试验;在研试验,针对RRMM的多项关键试验正在进行中,包括MagnetisMM-5、MajesTEC-3、MajesTEC-9等,预计近1-2年会逐步公布临床研究结果。
七、结语
综上所述,2026年ASCO指南的发布标志着多发性骨髓瘤治疗正式迈入“四药时代“和”免疫治疗时代“,构建了从SMM选择性干预到复发患者T细胞重定向治疗的全程管理框架。然而,指南推荐并非一成不变的教条,共享决策是贯穿始终的核心,在诸多有效选择面前,患者应积极参与治疗决策,综合考虑疗效、毒性、便利性、生活质量和个体价值观。动态指南机制的引入确保了临床实践能够紧跟证据演进的步伐,对于患者和家属而言,这意味着希望的不断延续;对于临床医生而言,这既是机遇也是挑战——在快速变化的证据海洋中,如何为每一位患者找到最优的个体化方案。多发性骨髓瘤的治疗仍在路上,随着MRD驱动治疗策略的成熟、新型免疫治疗的迭代以及疾病生物学理解的深入,”治愈“这一终极目标或许已不再遥远。[1] Mikhael J, Ismaila N, Cheung MC, et al. Treatment of Multiple Myeloma: ASCO and CCO Joint Clinical Practice Guideline. J Clin Oncol. 2019 May 10;37(14):1228-1263. doi: 10.1200/JCO.18.02096. Epub 2019 Apr 1. Erratum in: J Clin Oncol. 2020 Jul 20;38(21):2469. doi: 10.1200/JCO.20.01626.[2]Hicks LK, Messersmith HJ, Al Hadidi S, et al. Treatment of Multiple Myeloma: ASCO-Ontario Health (Cancer Care Ontario) Living Guideline. J Clin Oncol. 2026 Jan 6:JCO2502587. doi: 10.1200/JCO-25-02587.


 图3. 关键随机对照试验(RCT)的研究结果和证据质量
图3. 关键随机对照试验(RCT)的研究结果和证据质量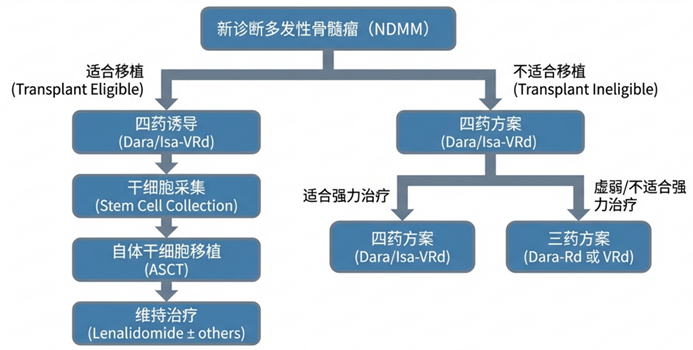
 图5. 双特异性抗体关键特征及治疗效果
图5. 双特异性抗体关键特征及治疗效果