药融云数据www.pharnexcloud.com监测显示:近日,浙江华海药业股份有限公司的下属子公司上海华奥泰生物药业股份有限公司及华博生物医药技术(上海)有限公司收到国家药品监督管理局核准签发的注射用 HB0052 的《药物临床试验批准通知书》。

一、药物基本情况
药物名称:注射用HB0052
适应症:晚期实体瘤
受理号:CXSL2400142
剂型:干粉制剂
申请事项:临床试验
申请人:上海华奥泰生物药业股份有限公司、华博生物医药技术(上海)有限公司
结论:同意开展临床试验
二、药物的其他相关情况
2023年11月,美国食品药品监督管理局(FDA)同意该药物开展临床试验, 近期,国家药监局同意该药物开展用于晚期实体瘤的临床试验。
截至目前的4月29日,公司在HB0052项目上已合计投入研发费用约人民币4,821万元。
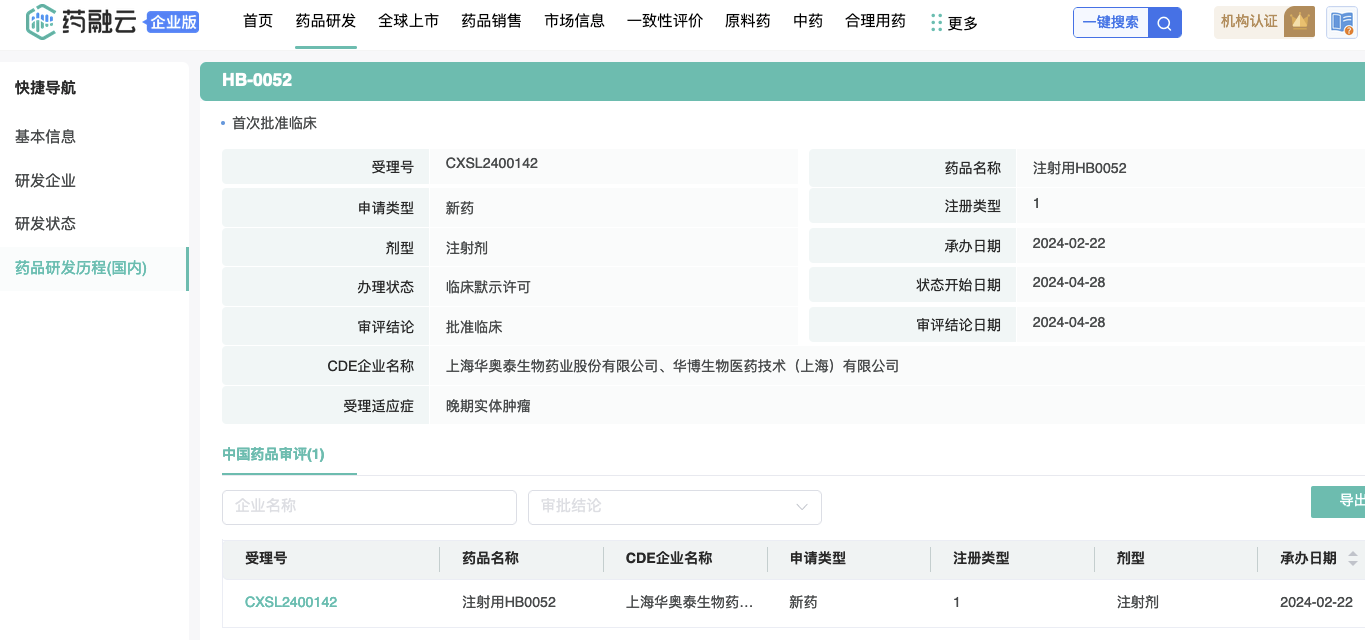
药融云数据www.pharnexcloud.com;国内时间轴
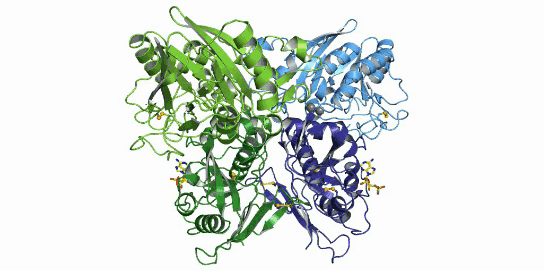
HB0052 是基于华奥泰抗体偶联药物平台研发的首款以拓扑异构酶抑制剂为载荷,靶向 CD73 抗原的第三代抗体偶联药物。该 ADC 分子能同时发挥抗体介导的免疫系统调节功能以及毒性小分子对肿瘤细胞的杀伤功能,具有协同抗肿瘤作用。临床前动物模型研究表明 HB0052 的抗肿瘤效果优异;非人灵长类动物中开展的临床前药代动力学结果显示HB0052 呈线性药代特征,血浆稳定性良好,非特异性脱落水平低,具有较长的半衰期和令人满意的药代动力学特性;毒理研究显示HB0052 安全性和耐受性良好。HB0052 有望成为新一代肿瘤治疗药物。
目前,国内外以CD73为靶点的药物均尚未上市。有多个单抗项目处于临床研究阶段,开发的适应症有非小细胞肺癌、乳腺癌、胰腺癌、前列腺癌等实体瘤。其中,阿斯利康研发的Oleclumab(抗CD73单抗)研发进度最快,目前处于III期试验阶段,用于同步放化疗后的不可切除NSCLC治疗。华奥泰的HB0052是全球第二个进入临床的CD73-ADC药物。
华海药业旗下华奥泰生物是一家以自主开发为主、着眼于全球的生物新药研发企业。专注于肿瘤、自身免疫疾病和眼底病变等领域生物新药的研发,目前已有11个项目在临床阶段:包括已经进入关键临床,国内首家本土自研针对脓疱型银屑病(罕见病)的IL-36R单抗;和目前临床II期,在子宫内膜癌和肾癌,晚期肺癌等多个肿瘤疾病中观测到积极信号的PD-L1/VEGF双抗;首个具有双重杀伤作用并针对胰腺癌等难治性肿瘤的CD73-ADC等核心项目。
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 南京市江宁区科学园乾德路5号