基因治疗让我们能够治疗“无法治愈”的疾病,也为其他疾病带来新的治疗思路。目前基因治疗的主要应用场景是治疗罕见病,随着AAV递送系统不断成熟,基因治疗“⼀次给药”的特性对病⼈吸引力越来越大,越来越多的在研管线将应用场景从罕见病拓展到常见病。
目前超70%基因递送药物均采用AAV载体递送,AAV递送的基因或基因组不会整合进自体基因组,因此AAV递送的基因有可能会随着细胞的分裂、死亡或者其他原因不断被稀释从而导致疗效不能持久。所以基因疗法的耐久性问题也一直备受关注。
基因疗法因其光明前景和巨大商业潜力已经成为了各大药业巨头寸土必争之地。
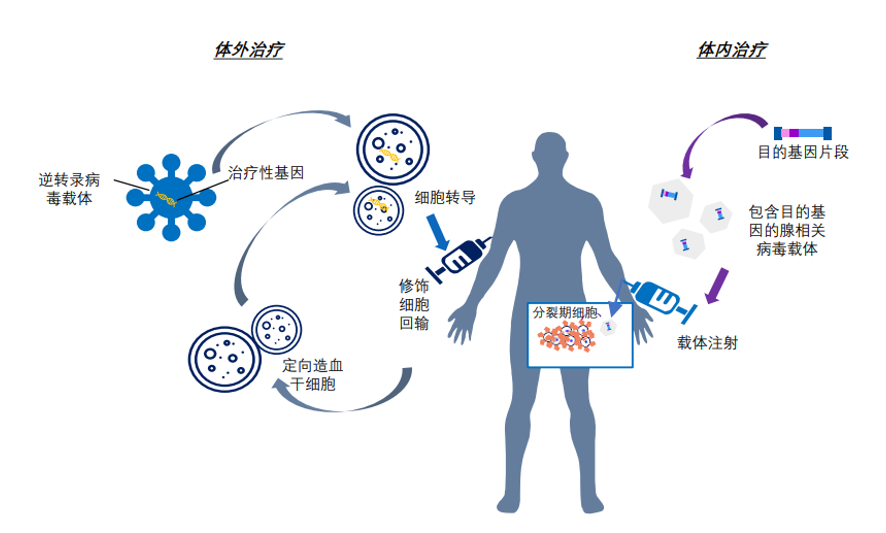
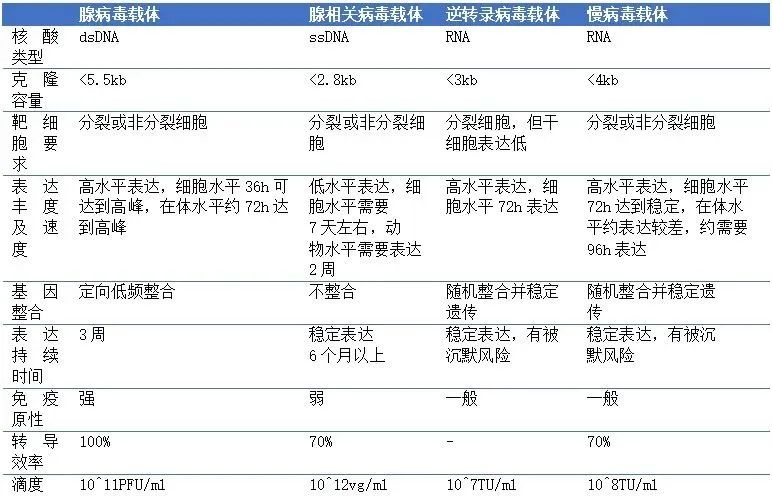
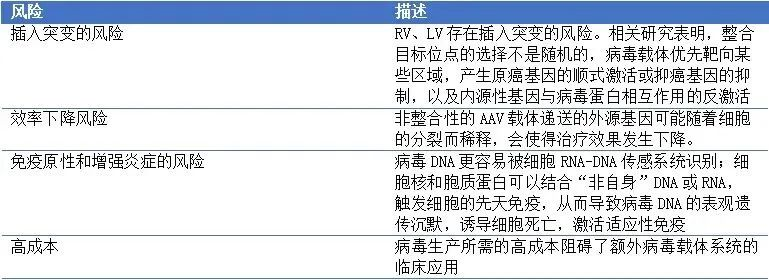
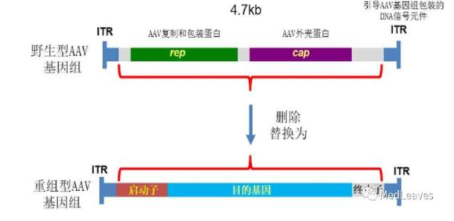
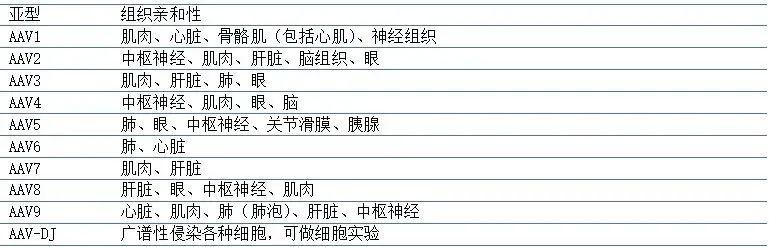
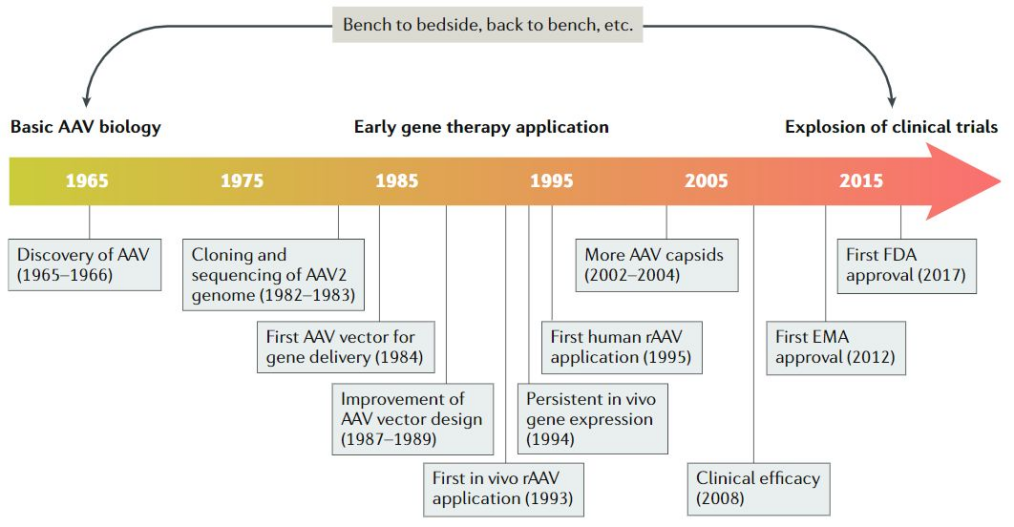
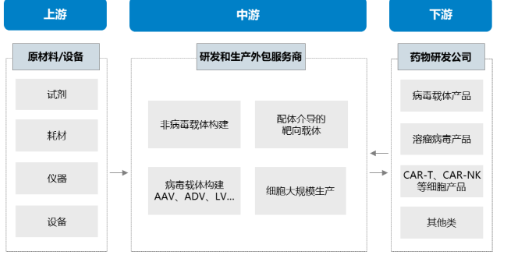
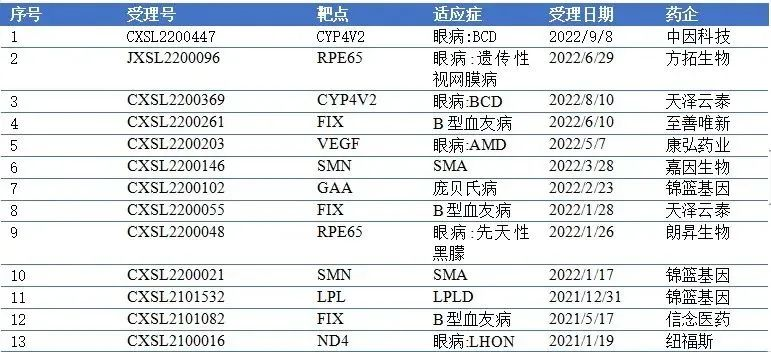
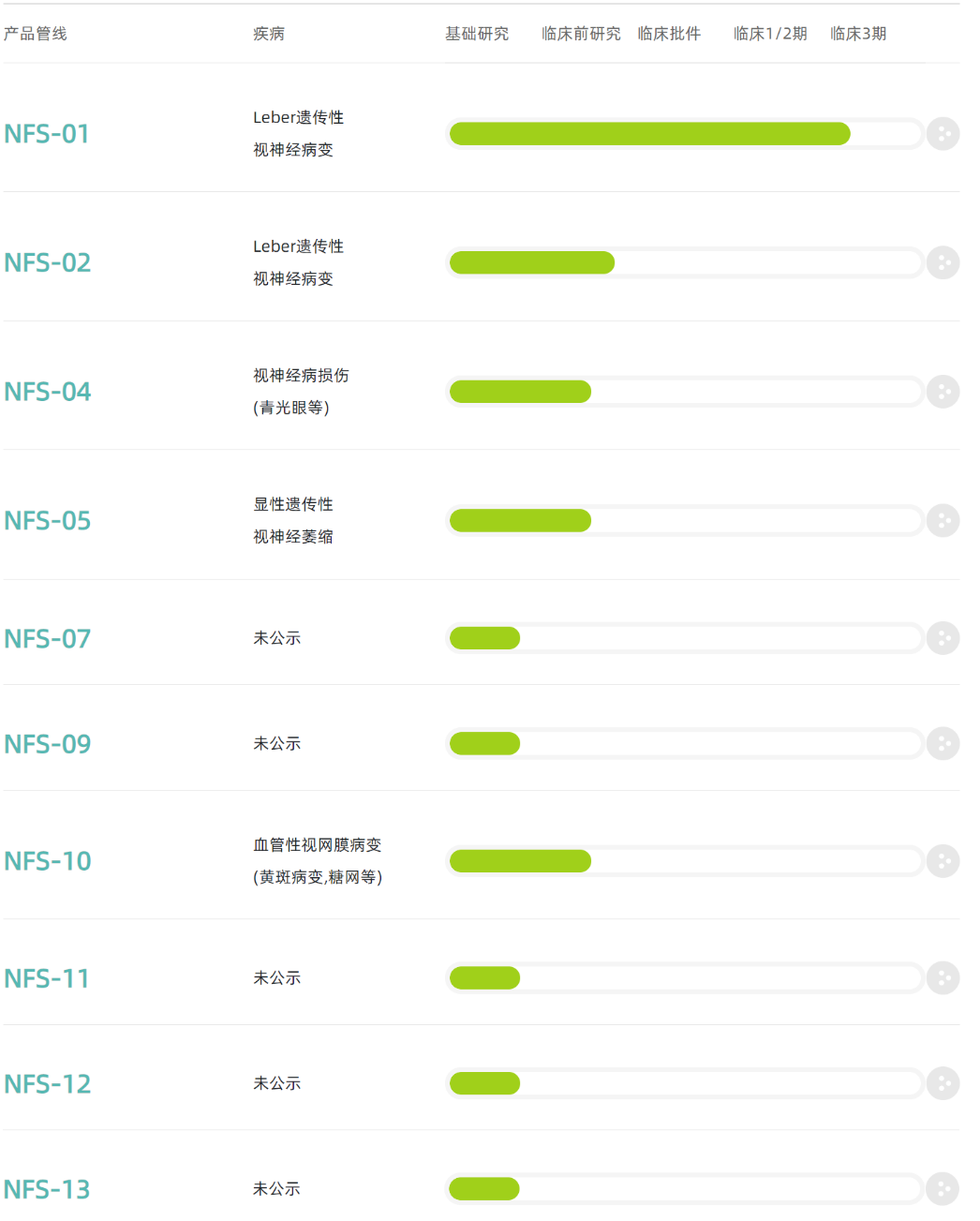
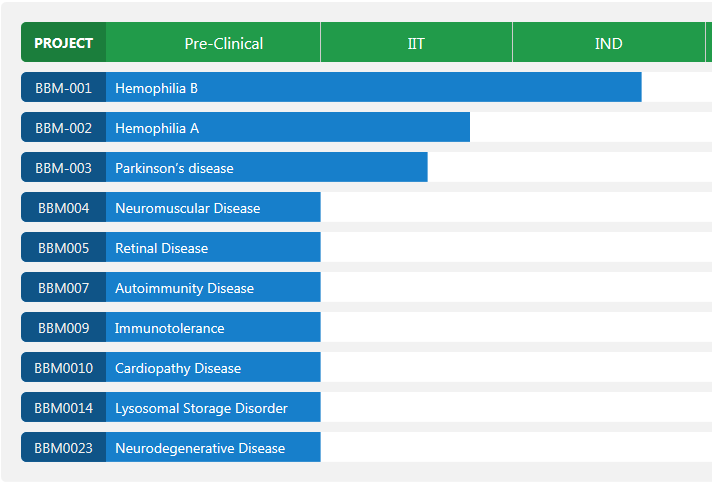
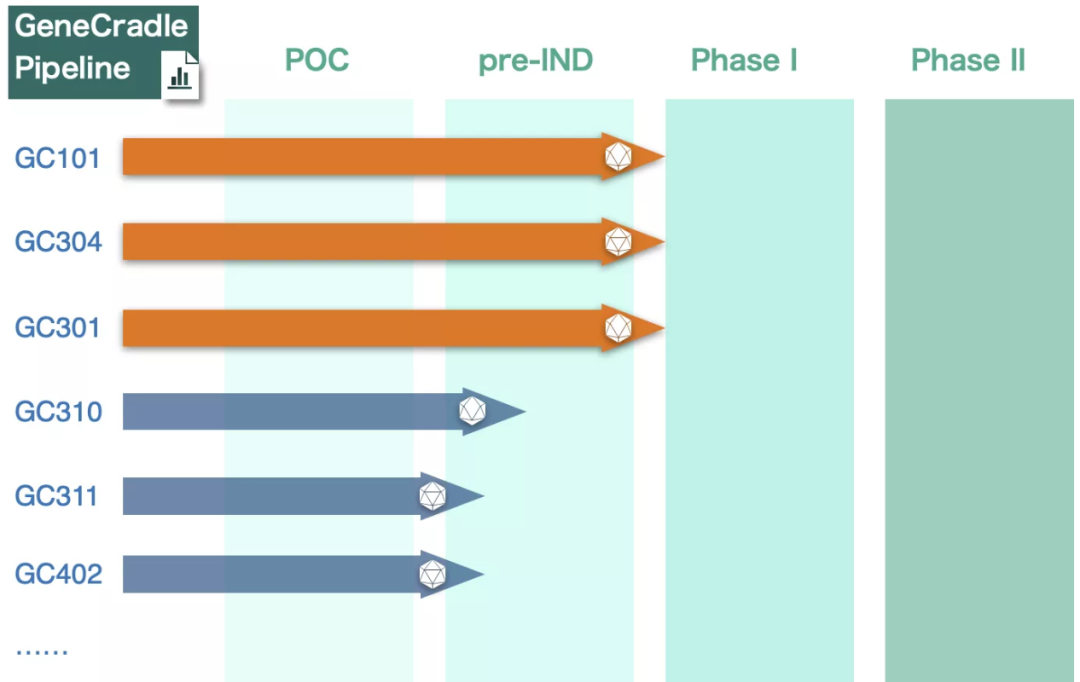
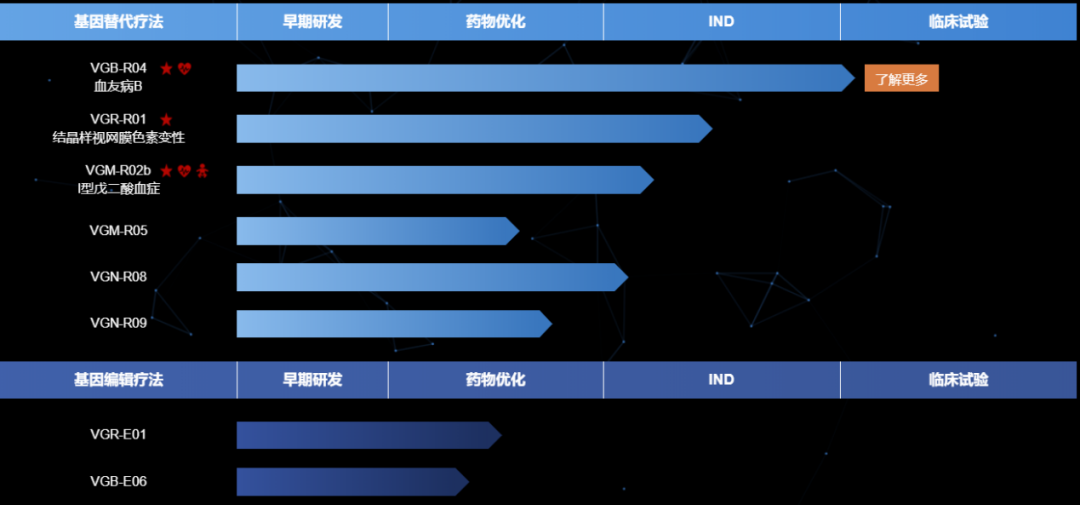
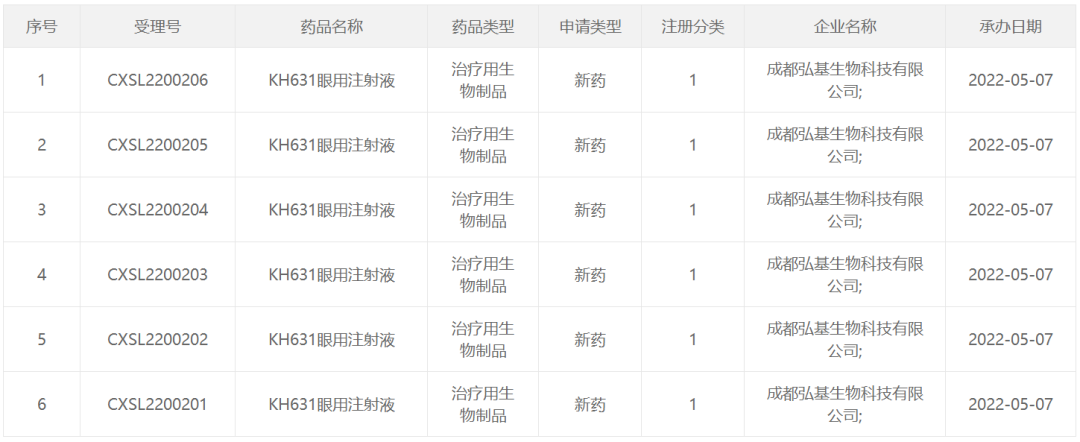
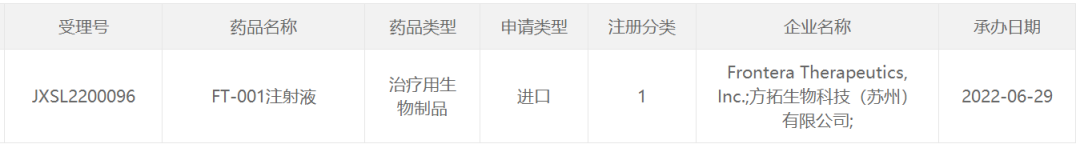
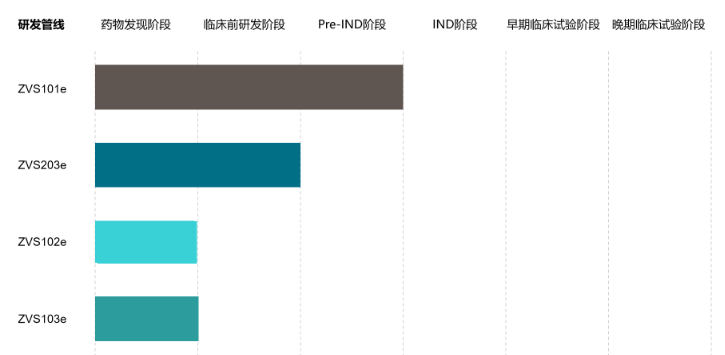
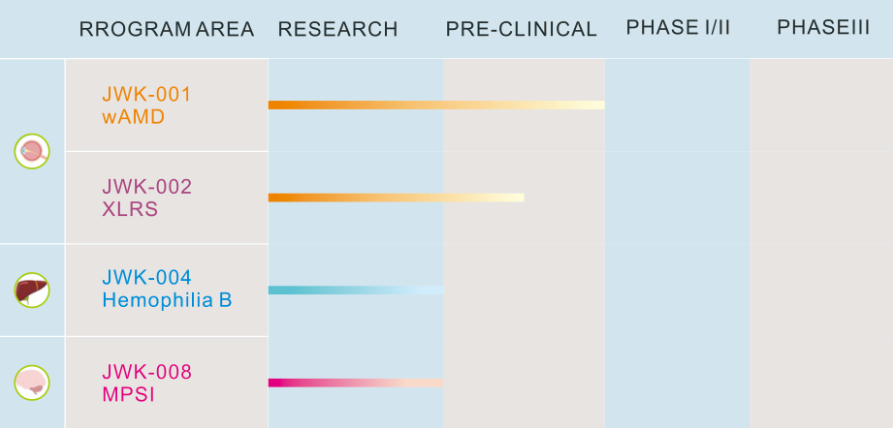
溶瘤病毒:指天然存在或经基因工程改造后,具有选择性的在肿瘤组织内复制、杀伤肿瘤细胞,但对正常组织无伤害的病毒。利用溶瘤病毒开发出的肿瘤治疗药物被称为溶瘤病毒药物。基因治疗:是指通过基因添加,基因修正,基因沉默等方式修饰个体基因的表达或修复异常基因,达到治愈疾病目的的疗法。病毒载体:是一种常用的分子生物学工具,可将遗传物质带入细胞,原理是利用病毒具有传送其基因组进入其他细胞进行感染的分子机制。AAV: 腺相关病毒, 也称腺伴随病毒,属于微小病毒科依赖病毒属,是目前发现的一类结构最简单的单链DNA缺陷型病毒,需要辅助病毒参与复制。基因治疗是一种利用基因治疗载体将外源的治疗性基因转导至细胞,再通过外源基因的转录和翻译,改变细胞原有基因表达以治疗疾病的方法。其作用方式一般包括:①用正常基因替代致病基因;②使致病基因失活;③导入新的或经过改造的基因。目前已上市和临床试验阶段的基因治疗产品主要靶向肿瘤、罕见遗传性疾病等适应症。基因治疗是继小分子、大分子靶向疗法之后的新一代精准疗法,为肿瘤、罕见病、慢病及其他难治性疾病提供了新的治疗理念和手段,具备了一般药物可能无法企及的长期性、治愈性疗效。基因疗法是指将功能基因递送到患者体内,以矫正或置换治病基因的一种治疗方法。在这种治疗方法中,目的基因被导入到靶细胞(target cells)内,他们或与宿主细胞(host cell)染色体整合成为宿主遗传物质的一部分,或不与染色体整合而位于染色体外,但都能在细胞中得到表达,起到治疗疾病的作用。1、基因修饰(gene augmentation):又称基因增补,将外源基因导入病变细胞或其它细胞,外源基因的表达产物能修饰缺陷细胞的功能或使原有的某些功能得以加强,是目前已上市和实验中的基因疗法最主要的作用原理之一。在这种治疗方法中,缺陷基因仍然存在于细胞内。在这一原理下,利用基因疗法具有长期表达和组织特异性表达治疗性蛋白的特点,有两种药物设计思路:(1)将基因疗法作为长效的给药方式,基于治疗性蛋白反向设计基因序列,完成药物设计,例如在wAMD中的应用;(2)将基因疗法作为一种全新的治疗方式,针对过去无法治疗或难以治疗的疾病,从基因出发设计药物,例如Luxtuma、Zolgensma。2、基因置换(gene replacement)/基因修复(gene correction):用正常的基因原位替换病变细胞内的致病基因,或定点导入外源正常基因替代缺陷基因(点特异性修复),使细胞内的DNA完全恢复正常状态。这种治疗方法在设计上最为理想,但技术上仍未突破,操作难度也极大,且用于生殖细胞时伦理争议极大。目前单碱基编辑技术(Base Editing)是该领域的宠儿,但还有一段很长的路要走。3、基因失活(gene inactivation):利用反义技术、核酶技术或基因敲除技术(knock-out)特异地封闭基因表达特性,抑制有害基因的表达。如反义RNA、核酶或RNAi等药物,有望在非一过性病毒感染及神经系统疾病。4、免疫调节(immune adjustment):将抗体、抗原或细胞因子的基因导入病人体内,改变病人免疫状态,达到预防和治疗疾病的目的。可从体液免疫和细胞免疫两个维度设计药物,例如CAR-T。根据治疗途径,基因治疗可分为体内基因治疗和体外基因治疗。其中体内基因治疗是指将携带治疗性基因的病毒或非病毒载体直接递送到患者体内,获批药物,如2019年经FDA批准的Zolgensma,是一种治疗脊髓性肌肉萎缩症的基于腺相关病毒载体的体内基因疗法;体外基因治疗则指将患者的细胞在体外进行遗传修饰后回输,获批药物如2017年FDA批准的Kymriah,是一种用于治疗难治或复发性B细胞前体急性淋巴性白血病(ALL)的基于慢病毒载体的体外基因疗法。主要包括基因治疗载体产品、基因修饰的细胞产品,以及具有特定功能的溶瘤病毒产品。基因产品包括细胞、溶瘤和载体,本报告聚焦于AAV载体治疗产品。基因治疗的递送,目前有两种解决思路:机械和物理递送以及基于载体的基因递送。非病毒载体递送主要是考虑到病毒载体安全性、治疗性DNA容量以及成本等问题,目前非病毒载体包括质粒或裸露DNA(非病毒)、LNP递送系统等,但体内转染效果差以及毒性过大严重制约了非病毒载体的临床转化。病毒载体则包括常用的腺相关病毒AAV、慢病毒LV和逆转录病毒RV等载体。优质的病毒载体应具备有足够的空间来递送大片段的治疗基因;具有高转导效率,能感染分裂和非分裂的细胞;能靶向特定的细胞,且可以长期稳定表达转基因;具有较低的免疫原性的或致病性,不会引起炎症;具备大规模生产的能力等优点。n人工改造的病毒是目前基因治疗中最常用的载体。病毒载体优化升级则贯穿了整个基因治疗的发展史,感染效率更高、安全性更好的病毒载体的使用也是近年基因治疗取得成功的关键动因。目前常用的四种病毒载体各有优缺点,适用于不同场景。AAV和LV分别是基因和细胞治疗的新一代载体,相比前代的ADV和RV具有免疫原性弱、能够穿透核膜的优势。AAV和LV对比:LV有更强的嗜性,能够感染非分裂细胞,同时在安全性上较RV更安全;AAV的宿主范围极为广泛,长时程基因表达,治疗效果持久,同时其免疫原性极低,肝毒性低,但包装容量小、感染到表达的时间比较长。AAV是一种无包膜单链DNA病毒,属于细小病毒家族。AAV作为最早通过欧盟FDA认证的基因治疗载体,因其具有宿主范围广、非致病性、低免疫原性、长期稳定表达外源基因、良好的扩散性能和物理性质稳定等优点,已被广泛地应用于基础研究和临床试验中。目前己发现AAV有12种亚型及120多种变型,并逐步用于基因药物研发。rAAV携带的蛋白衣壳与野生型AAV几乎完全相同,然而衣壳内的基因组中编码病毒蛋白的部分被删除,取而代之的是治疗性转基因(transgene)。AAV基因组中唯一被保留的部分是ITRs,它起到指导基因组的复制和病毒载体组装的作用。将编码病毒蛋白删除,一方面可以最大化重组AAV携带转基因的容量,另一方面可以减小病毒载体的免疫原性和细胞毒性。传统药物是直接补充人体所需的重要物质(蛋白质、无机物、多肽等等)或调节信号通路中的蛋白靶点,基因疗法的作用位点更“上游”,在核酸水平上开展治疗。理论上由蛋白质异常导致的疾病,都可以通过核酸的作用来治疗,基于此,基因疗法可治疗的领域非常广泛,一些过去无法治疗的疾病有了解决方案,一些给药痛苦且频繁的疾病有了改善方案,重点体现在以下三类疾病:1、遗传性疾病:受限于技术,目前主要应用领域还是单基因遗传病,如SCID、镰刀状贫血、血友病、地中海贫血、苯丙酮尿症等。治疗原理是基因修饰,由于单基因突变的存在,靶细胞会产生异常蛋白或不产生正常蛋白,基因疗法通过病毒载体将外源基因导入到靶细胞内,以表达正常蛋白,达到治疗目的。2、恶性肿瘤:治疗原理包括基因失活、免疫调节、自杀基因,进展最靠前的是免疫调节,包含3个已上市的CAR-T药物,通过对T细胞表面的识别蛋白进行改造,从而激活细胞免疫。3、需长效作用的疾病:这里特指非遗传但治疗过程中需要长效作用的疾病,比如wAMD、干眼,应用基因转导长效分泌蛋白质,达到一次给要长期有效,大幅减轻给药痛苦,也有减少总治疗费用的可能。药物递送系统(Drug Delivery System,DDS,药物传递系统)是指在空间、时间及剂量上全面调控药物在生物体内分布的技术体系。其目标是在恰当的时机将适量的药物递送到正确的位置,从而增加药物的利用效率,提高疗效,降低成本,减少毒副作用。小分子药物是最主要的治疗药物,但是它们的递送很大程度上取决于它们本身结构的物理化学性质,这严重影响药物的生物利用度,因此提高药物的溶解度,控制它们的释放,优化它们的活性以及改善它们的药代动力学是首先要解决的递送问题。随着时间的推移,新一代的治疗方法不断涌现,包括蛋白质、多肽、单克隆抗体、核酸和活细胞等,这些方法提供了新的治疗功能。但是新的功能不可避免的带来了新的挑战,比如蛋白质和多肽稳定性问题,核酸往细胞内递送的效率问题以及活细胞的活力和扩增问题等等。病毒才是导弹级别的递送系统――绝大多数病毒都有精确到极致的细胞识别能力。流感病毒,它就只会识别人体的呼吸道上皮细胞。而乙肝病毒,它就只会识别人体的肝脏细胞,这种精确识别的背后原理实际作为药物投递系统其精确度可能远超过人类世界发明出的所有人工系统。迄今为止,除了Glybera,获批上市的基因药物共有五个:分别是Luxturna(AAV)、Zolgensma(AAV)、Yescarta和Kymriah(均为CAR-T细胞疗法)、 Imlygic(溶瘤病毒载体)以及Strimvelis (伽马逆转录病毒),其中三个应用的是AAV载体。另外还有数十种治疗方法处在临床试验阶段。各种形式的临床基因治疗也正在迅速发展。这其中最被看好的病毒载体就是AAV,因为AAV具有良好的安全性和较高的递送效率。20世纪60年代中期从实验室腺病毒制剂中AAV被发现,随后很快在人体组织中找到。此后的15到20年间, AAV的生物学特性也逐一被揭晓,包括AAV的基因构型和组成、DNA复制和转录、感染潜伏期和病毒颗粒包装,这些研究结果共同促进了野生型AAV2序列成功克隆到质粒中,实现了基因研究和整个AAV2基因组测序,为AAV作为基因递送载体提供了基础知识。1984年,首个用于基因递送的rAAV载体问世,随后rAAV载体设计有了进一步的发展并开始在体内应用。1994年和1995年分别实现了体内的持续表达和在人体中的应用。2002年开始,更多的衣壳陆续被发现。近十年来,基于AAV的基因治疗药物有了重大突破,相关药剂分别于2012年和2017年被EMA和FDA认证。2017年12月,美国FDA批准罗氏旗下Spark Therapeutics公司的眼科基因疗法Luxturna,用于治疗一种可导致失明的遗传性视网膜疾病。2019年5月,诺华旗下AveXis的脊髓性肌萎缩症(SMA)基因疗法Zolgensma也获得FDA批准上市。上述产品是真正意义上的基因治疗产品,标志着基因治疗时代的正式来临。2022年2月,REGENXBIO公布了其眼科AAV基因疗法RGX-314的2期ALTITUDE试验的积极中期数据。2021年9月,艾伯维还曾以18亿美元引进了REGENXBIO的RGX-314。2022年5月25日,CSL Behring宣布,美国FDA已接受该公司为在研基因疗法etranacogene dezaparvovec递交的生物制品许可申请(BLA)并授予优先审评资格,用于治疗血友病B成人患者。2022年7月21日,PTC Therapeutics宣布,欧盟委员会批准基因疗法Upstaza(eladocagene exuparvovec)上市,用于治疗18个月以上芳香族L-氨基酸脱羧酶缺乏症(一种影响大脑的罕见遗传疾病),该法是直接注入大脑的首款获批基因疗法,也是改变该疾病进程的首款获批疗法。根据再生医学联盟(Alliance for Regenerative Medicine,ARM)的数据显示,2021年,基因和细胞治疗行业的投资总额达到了230亿美元,其中约一半的资金流入专门开发基因疗法的开发商。2021年12月22日,诺华宣布已完成对眼科AAV基因疗法公司Gyroscope Therapeutics的收购。此次收购的预付款就高达8亿美元,后续的里程碑付款为7亿美元,共15亿。2022年7月19日,Avista Therapeutics公司与罗氏签署了一项合作协议,开发用于眼部疾病的AAV基因治疗载体。根据协议,罗氏将预先向Avista支付750万美元,加上潜在的里程碑付款,该合作协议的潜在交易价值总计超过10亿美元。2022年7月22日,Vertex Pharmaceuticals和Verve Therapeutics宣布双方达成一项为期四年的独家合作关系,共同开发一种肝病领域的基因编辑疗法,具体的适应症尚未公开。根据协议,Vertex将向Verve支付6000万美元的预付款,此后,Verve将有资格获得高达6600万美元的成功付款、高达3.4亿美元的开发和商业里程碑付款以及未来销售的分层特许权使用费。根据Cortellis 2022年数据,共1563个使用病毒和质粒载体,其中,有824个AAV载体在研和已上市药物,203个腺病毒载体在研和已上市药物,106个逆转录病毒,54个慢病毒,24个疱疹病毒,87个质粒,其余为unspecified。可以看出,AAV载体为目前基因疗法开发利用的载体系列里最高频使用的一个载体,显著高于第二高频使用的腺病毒载体。一是载体容量比较小,二是感染到表达的时间比较长。但这些缺点目前还没有制约到AAV载体的产业应用,且AAV作为基因治疗的载体具有多种不可替代的优势。1)主要以附加体(非整合性环状表体)形式存在,不整合到宿主基因组中;4)血清型多,可选择性靶向不同的细胞、组织和器官;神经、眼科、代谢等领域是AAV载体治疗的主要领域。根据Cortellis 2022数据(数据未列示),目前所有在研针对眼科疾病的AAV疗法有152个,252款针对神经类疾病,170款针对代谢类疾病,65款针对骨骼肌,46款针对血液疾病。从Cortellis 2022年数据来看,包括辉瑞、罗氏、诺华、杨森、艾伯维等在内的大型跨国药企均布局了AAV基因疗法。神经、代谢和眼科领域均有超过100支管线,为AAV载体疗法重点应用的领域。已上市的两款药物中,一款是针对神经领域疾病,一款是针对眼科疾病。近20年AAV基因治疗在各领域的临床试验数量均有所增加,尤其是代谢性疾病和眼科疾病。在目前现有的临床试验中,有26%是针对眼科疾病进行的。2017-2021年范围内,代谢性疾病的临床试验数量增幅最大,眼科疾病、血液疾病和神经系统疾病的临床试验数量也在增加,而心血管疾病是唯一一类临床试验数量开始减少的疾病。眼睛是基因治疗理想的靶器官,在目前基因治疗领域中安全性和成功率均较高,原因在于眼部属于免疫豁免区域,是环境封闭的小组织靶点,患者所需的剂量通常较低,有助于更经济和更小规模的AAV制造策略。在美国,诺华的CAR-T细胞疗法药物Kymriah(tisagenlecleucel)针对复发或难治性B细胞急性淋巴细胞白血病(ALL)和复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)适应症,分别定价为47.5万美元和37.3万美元。Kymriah的竞争对手吉利德Yescarta定价为37.3万美元。2019年2月美国医疗保险和医疗补助服务中心(CMS)批准CAR-T细胞治疗纳入医保,以缓解患者的财务压力。除了美国,英国、以色列、加拿大、日本和意大利等国家也已经将Kymriah或Yescarta纳入医保范围。中国已获批的CAR-T疗法的主要费用是一次性发生的,疗效却要长期观察才能确定,然而目前我国医保是按服务项目付费的方式,是在医疗服务行为产生后按实际费用进行补偿,针对高昂的一性性医疗费用在我国尚未建立医保付费机制。目前各大保险公司都在紧锣密鼓地将CAR-T纳入商业保险的保障范围之内:复星联合健康保险公司旗下的两款医疗险产品“超越保2020医疗险”和“药神一号2021”均更新了“恶性肿瘤特药清单”,加入了CAR-T疗法阿基仑赛,无须付费,老客户自动享受更新。短期内,商业保险的补充,将是需要使用基因治疗的癌症患者的希望。随着基因治疗行业的火热,基因治疗CDMO成为产业结构优化的必然选择。主要原因有两点:一方面中国基因治疗不仅吸引大量的药企纷纷布局,一些小型企业也大量涌现,但是小型企业在研发方面缺乏足够的经验,也没有配套的生产设备,因此对基因治疗CDMO企业的需求很大。另外一方面,CDMO企业作为专业的研发外包企业,其专注于研发的某一环节,因此其专业性,效率等都比制药企业具有优势。AAV载体产品属于CGT的其中一部分,因此本报告对于AAV产业链描述借鉴CGT行业中的CDMO行业。基因治疗本身具有技术机制复杂、工艺开发门槛高、法规监管要求严格、商业化经验有限、大规模生产限制繁多等特点,相比传统的大分子和小分子制药,基因治疗行业对CDMO服务更为依赖,选择CDMO服务能够为基因治疗新药研发企业减少成本和降低风险。基因治疗产业链上游主要为设备、仪器、试剂耗材供应商,下游主要为基因治疗新药研发公司。上游:CGT疗法蓬勃发展,上游装备耗材国产化大有可为,例如。国内近年来在CGT产业的快速发展背景下,上游的设备、耗材市场已出现增长。但因为国内产业起步较晚,部分中高端设备依然以进口为主,国内企业的细胞培养及开发工艺、离心提取、分离收集、无菌连接系统等工艺技术与外资企业存在较大的差距。未来国产企业还需要不断加强工艺技术研发能力和服务能力,才能加快进口替代步伐,赢得市场机遇。中游:细胞基因治疗生产具有高壁垒,CDMO企业通过专业化分工实现赋能。CGT生产可分为质粒工程、病毒工程、细胞工程三个较为独立的部分,各自难点不一,在质粒构建、菌库构建、递送系统设计、细胞系构建、细胞培养等环节,药企与CDMO企业间存在技术互补。当前CGT领域技术迭代速度快,企业前期投入较大且风险较高,选择CDMO服务不失为明智策略。下游:细胞基因治疗逐步从基础科学研究转化到工业应用,得到市场的广泛认可和重视。CDMO产业的下游主要为各类药物研发公司客户,使用产品包括质粒、病毒载体、细胞产品等。细胞基因治疗产品的终端则是以三级医院为主的各类医疗机构。全球范围内,累计有3款AAV基因疗法获批上市,2012年欧盟批准的Glybera(未获FDA批准),2017年FDA批准Luxturna,但这两款药物市场层面都不算成功。诺华的Zolgensma于2019年获得批准,获得了巨大的商业成功,2021年销售额13.51亿美元,今年上半年销售额7.42亿美元。国内方面,已经累计申报13款AAV基因疗法,其中2021年3款,2022年10款,呈快速增长的趋势。纽福斯成立于2016年,创始人为李斌教授。纽福斯聚焦于眼病治疗领域,而不局限于AAV疗法。2022年6月,纽福斯与艾博生物达成合作,开发治疗眼病的mRNA疗法。已完成5轮融资,C轮融资4亿元人民币,投资机构包括国投招商、红杉中国、阳光人寿、招银国际资本。信念医药成立于2019年,创始人为北卡大学的肖啸教授,也是基因治疗领域权威专家。信念医药已经建立了丰富了研发管线,包括针对血友病、帕金森、眼病等多种适应症的基因疗法。信念医药首发管线BBM-H901的适应症为B型血友病,获得国家药监局的突破疗法认证。已完成3轮融资,B轮融资6.8亿美元,启明创投、经纬创投、夏尔巴投资、晨岭资本、礼来亚洲基金、千骥资本。锦篮基因成立于2018年,核心技术团队作为国内最早进入基因治疗及其核心技术“病毒载体系统”领域的国家队原班人马,出自侯云德院士领导的病毒基因工程国家实验室病毒载体课题组。创始人吴小兵教授为国内第一个申请临床的AAV基因治疗药品的首席科学家。锦篮基因已经申报3款AAV基因疗法,分别为治疗LPLD的GC304、治疗SMA的GC101和治疗庞贝氏病的GC301。完成4轮融资,A轮融资2亿元人民币,股东包括,华金资本、亦庄国投、东方富海、赛盈资本、深创投、康居基金、屹唐华睿、凯乘资本。朗信生物成立于2020年,聚焦于眼病AAV基因疗法,创始人兼CEO汪枫华为上海市眼科工程技术研究中心主任,联合创始人兼CTO张瑰宜此前为Regenxbio的工艺开发总监。朗信生物的首发管线LX-101为AAV2搭载RPE65基因,用于治疗LCA。天泽云泰成立于2020年,创始人为赵小平(原益诺思(海门)生物总经理)和李伟(中科院动物所研究员)。天泽云泰已经申报2款AAV基因疗法,分别为治疗B型血友病的VGB-R04、治疗结晶样视网膜色素变性的VGR-R01。已完成3轮融资,股东包括,临港蓝湾基金、高瓴创投、千骥资本。杭州嘉因生物成立于2019年,首发管线EXG001-307最近刚刚获批临床,为国内首款治疗SMA的AAV基因疗法。已完成4轮融资,B++轮融资数千万美元,股东包括高瓴资本、CPE源峰、Temasek淡马锡、清池资本、洲嶺资本、博远资本。康弘药业为A股上市公司,截至2022年10月30日,市值161亿元,2021年收入为36亿元。康弘药业申报的KH631为表达VEGF的眼病AAV基因疗法,即表达康柏西普的AAV疗法。至善唯新成立于2017年,创始人为四川大学华西医院生物治疗国家重点实验室董飚教授。前不久,君实生物入股至善唯新。至善唯新的首发管线ZS801为治疗B型血友病的AAV基因疗法。已完成3轮融资,A轮融资数亿人民币,股东包括正心谷资本、晨兴创投、德联资本、君实生物、磊梅瑞斯、川创投。芳拓生物2019年9月,汇聚了中美两地具有丰富创新基因药物研发、生产、注册、临床研究管理经验的专业人员,聚焦罕见病及慢性疾病领域,致力于研发和生产高质量的、患者可支付的重组腺相关病毒(rAAV)载体基因治疗产品,以满足全球遗传性和慢性病患者远未被满足的临床治疗需求。芳拓生物首发管线FT-001是一款针对RPE65基因变异导致的遗传性视网膜病的AAV基因疗法,已经获得FDA的临床许可,以及NMPA的受理。已完成2轮融资,B轮融资1.6亿美元,股东包括,博裕资本、红杉中国、正心谷资本、史带资本、奥博资本、泓元资本。中因科技有限公司是一家专业从事遗传性眼病临床基因诊断、预防和基因治疗药物研发的企业。首发管线ZVS101e主要是使用rAAV病毒将正常的CYP4V2基因拷贝携带到患者视网膜细胞中,治疗结晶样视网膜变性。已完成5轮融资,A轮融资亿级人民币,股东包括龙磐投资、盈科资本、华医资本、隽赐投资。北海康成成立于2012年,是一家总部位于中国、专注于全球罕见病的领先生物制药公司,致力于变革性疗法的研究、开发和商业化。成立于 2019 年 8 月,位于安徽省合肥市,公司聚焦眼科疾病的基因治疗药物开发和基因编辑技术研发、服务,致力于开发中国人自主可用的眼科基因治疗药物,让中国人看得更久,看得更好。wAMD管线已经实现体内体外药效显著优于美国头部产品RGX-314,并配合自有的新衣壳在该领域实现了玻璃体腔注射的术式。除了进度最快的wAMD管线之外,星眸生物在青光眼,甲状腺眼病,非青光眼性失明,以及干性AMD方面也有布局。已完成2轮融资,Pre-A轮融资近亿人民币,股东包括国科投资、中科创星、伊西尔丁、合肥高投、合肥产投集团、兴泰资本。金唯科成立于2017年,是一家致力于眼科疾病、神经肌肉疾病、遗传代谢疾病等的AAV基因治疗新药研发公司,拥有AAV基因治疗完整的研发平台及丰富的AAV基因治疗药物产品管线,基因治疗药物的科研能力以及AAV制备技术处于国内领先水平。治疗湿性老年性黄斑变性(wAMD)的JWK001和治疗X连锁青少年视网膜劈裂症(XLRS)的JWK002作为龙头管线,进展最快,将先后申报IND。
Pre-A轮融资数千万元人民币,股东包括睿景基金盈科资本、东湖高新、小明投资、四川绘素。虽然目前基因治疗产业尚处于发展前期,各方面都还不够完善,但随着未来适应症的不断拓展、基于人群扩大带来的市场的不断拓宽、技术成熟带来的成本下降以及医保支付条件的不断成熟等,基因治疗价格将会逐步下降惠及更多患者,治疗潜力也将不断释放,成为具有巨大市场张力的创新诊疗方法。在监管规范和政策支持下,国内基因治疗行业有望实现“弯道超车”,提升国内生物医药产业的整体创新能力和前沿领域影响力。根据弗若斯特沙利文的数据显示,2025年我国基因治疗市场规模将达到179亿元左右;假设在2025-2027年之间,我国基因治疗CAGR增速与全球保持一致,我国基因治疗市场规模将达到500亿元左右。基因疗法的发展经历了起伏和挑战。UniQure的第一个商业化基因疗法Glybera于2012年上市。但由于患者极少、价格极高且运营费用居高不下,Glybera于2017年退市。基因疗法的前景受到质疑。而随着时间的推移,更多基因疗法成功商业化,为该行业带来了新的关注。如基因疗法Zolgensma和Luxturna已在全球多个国家上市,其销售额已经超过一些传统主流治疗药物。以国内首个获批上市的CAR-T细胞治疗产品——复星凯特的奕凯达为例,截至2022年5月,奕凯达已成功进入32个省市的城市惠民保产品,预计覆盖人口超千万。以2022年上海沪惠保为例,投保人一旦发病并符合CAR-T治疗标准,即可获得最高50万元人民币的理赔,这大大降低了患者本人的经济负担,打开了市场容量。基因治疗已经成为全球最具发展潜力的医药领域之一,随着国家和各地政府的支持和促进,生命科学技术不断迭代升级,这些为细胞与基因治疗的发展都提供了持续的动力。涉及细胞与基因治疗相关领域的机构通过收购、合作开发、自主研究等形式共同推动基因治疗的发展,使得基因治疗已逐步走向快速发展的黄金赛道。