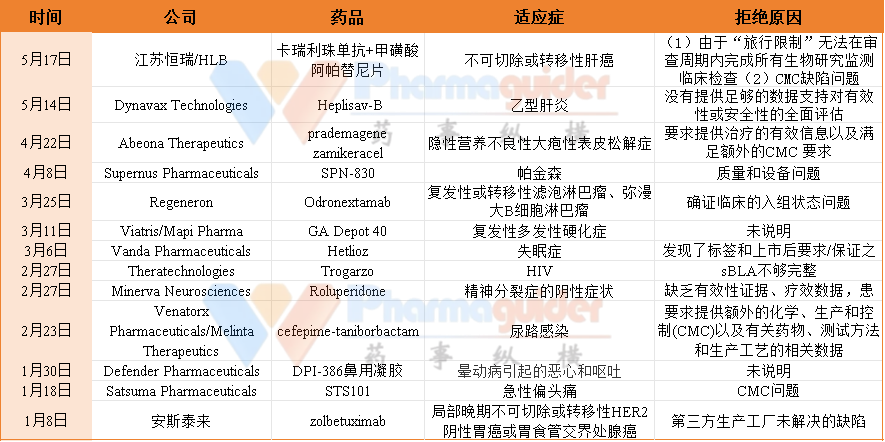
美国FDA的认证意味着产品的安全性和质量得到了权威性的认可和保证,能够为消费者提供更加可靠的产品,是产品品质与效果的全球最高标准证明,FDA一直致力于履行其促进和保护公众健康的使命。2024年1-5月FDA拒批了13款药物,小编整理如下:
5月17日,Elevar Therapeutics子公司HLB及其在中国的合作伙伴江苏恒瑞医药宣布收到FDA对于注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片用于不可切除或转移性肝细胞癌患者的一线治疗的BLA申请的完整回复信(CRL),在CRL中FDA表示会对恒瑞提交的生产现场检查缺陷完整回复进行全面评估,以及由于部分国家的旅行限制,无法在审查周期内完成必需的生物学研究监测计划(BIMO)临床检查,因此该产品的BLA申请将被拒绝。对此,恒瑞表示将尽快重新提交申请。

卡瑞利珠单抗(camrelizumab)是恒瑞医药研发的人源化抗PD-1单克隆抗体,于2019年5月在中国获批上市,此前已在肺癌、肝癌、食管癌、鼻咽癌以及淋巴瘤五大瘤种中获批了9个适应症。阿帕替尼(rivoceranib)是恒瑞医药开发的一款针对血管内皮生长因子受体(VEGFR)的小分子酪氨酸激酶抑制剂,于2014年10月在中国获批上市,目前有3个适应症获批,分别为单药用于晚期胃腺癌或胃食管结合部腺癌、既往接受过至少一线系统性治疗后失败或不可耐受的晚期肝细胞癌、联合卡瑞利珠单抗用于不可切除或转移性肝细胞癌。2021年4月,卡瑞利珠单抗联合阿帕替尼一线治疗不可切除或转移性肝细胞癌适应症获得FDA孤儿药资格。Dynavax Technologies 宣布 FDA 拒绝了其重组蛋白乙型肝炎疫苗用于在血液透析中患者的补充生物制品许可证申请。
这家加州生物制药公司表示,它收到了监管机构关于其sBLA的完整回复函(CRL),其中包括来自119名接受血液透析的成人的四剂量Heplisav-B方案的I期HBV-24研究的临床免疫原性和安全性数据。根据CRL,“申请没有提供足够的数据来支持对有效性或安全性的全面评估。”

FDA 认为该申请没有提供足够的数据来支持有效性或安全性的全面评估。CRL表示,HBV-24的数据不足,因为第三方临床试验现场运营商销毁了大约一半参加试验的受试者的数据源文件。该公司还透露,FDA发现单臂研究中的受试者总数“不足以评估四剂方案的安全性”。
Dynavax在其新闻稿中表示,FDA拒绝其sBLA不会影响欧盟委员会于2023年10月批准血液透析患者四剂量方案的决定,或Heplisav-B在美国、欧盟和英国被批准用于预防所有已知乙型肝炎病毒亚型引起的成人感染的适应症。4月22日,Abeona Therapeutics宣布FDA针对其细胞疗法 prademagene zamikeracel (pz-cel,EB-101)的完整回复信 (CRL),FDA拒绝了该疗法上市,并要求其提供治疗的有效信息,以及满足额外的CMC 要求才能批准申请。受此消息影响,Abeona股价大跌53%。
Pz-cel是一种体外基因校正的自体细胞疗法,用于治疗RDEB患者。该疗法由表皮片组成,旨在将功能性COL7A1基因传递到患者自身的皮肤细胞中,以实现正常的VII型胶原蛋白表达,并促进伤口愈合。
试验表明,pz-cel可以帮助治愈伤口,并减轻RDEB患者的疼痛。然而,FDA对其位于俄亥俄州克利夫兰的制造工厂进行检查,因 pz-cel 制造相关的问题,FDA驳回了pz-cel的上市申请,但没有要求提供额外的试验或数据来支持后续申请。pz-cel原定PDUFA 日期是2024年5月25日,现在将有所推迟。
4月8日,FDA宣布Supernus Pharmaceuticals治疗帕金森病的药物SPN-830第二次被拒,原因是质量和设备问题。SPN-830是一种阿朴吗啡注射剂,用于持续治疗帕金森病(PD)的运动波动(间歇性发作)。受此影响,Supernus股价在盘前下跌了10%。CRL中表示有两个方面需要FDA进行更多审查。第一个问题是Supernus需要提供更多信息,包括有关产品质量的更多信息。Supernus指出最近向监管机构提交了更多的产品质量数据,但尚未得到审查。FDA 提出的另一个问题与输液设备的主文件有关。Supernus 表示,主文件是专有的,并计划与设备制造商讨论监管机构要求的信息和重新提交 NDA 所需的步骤。与此同时,Supernus公司表示,没有发现任何临床安全性或有效性问题需要获得批准。
3月6日,Vanda Pharmaceuticals宣布,已经收到FDA就Hetlioz(他司美琼)治疗失眠补充新药申请(sNDA)发出的完整回应函。FDA表示发现了标签和上市后要求/保证之外的缺陷,不能批准目前的sNDA。Vanda正在对其进行审查,并评估下一步行动。

Hetlioz是一款褪黑素受体激动剂,2014年1月在美国获批治疗非24小时睡眠觉醒障碍。2020年12月,该产品拓展新适应症,获FDA批准治疗史密斯-马吉利综合征 (SMS) 夜间睡眠障碍。
Viatris/Mapi Pharma:GA Depot3月11日,晖致(Viatris)和Mapi Pharma共同宣布收到FDA就GA Depot(醋酸格拉替雷,40mg)用于治疗复发型多发性硬化症的新药申请(NDA)发出的完整回复函(CRL)。关于FDA拒绝的具体细节很少,这两家公司仅表示,他们目前正在审查完整回复函,以更好地确定GA Depot 40的“适当下一步”。
GA Depot 40的活性成分醋酸格拉替雷是一种免疫调节剂,1996年在美国获批用于治疗多发性硬化症(MS),商品名为Copaxone。2023年6月,格拉替雷在中国获批上市。GA Depot的NDA主要是基于一项III期研究的积极结果。该研究评估了GA Depot对比安慰剂治疗RMS患者的有效性、安全性和耐受性。结果显示,GA Depot组患者的年复发率相比安慰剂组降低了30.1%(P=0.0066)。2月27日,Minerva Neurosciences宣布收到FDA就Roluperidone用于治疗精神分裂症阴性症状的新药申请(NDA)发出的完整回复函(CRL),表示拒批其精神分裂症新药。受此消息影响,Minerva股价大跌59%。在CRL中,FDA 指出了以下四点拒批理由:虽然MIN-101C03研究在主要疗效终点上显示出统计学意义,但其本身不足以确立实质性的有效性证据;提交的NDA缺乏有关同时服用抗精神病药物的数据;NDA材料缺乏证明Roluperidone对改善精神分裂症阴性症状具有临床意义的必要数据;在已提交的安全性数据中,至少服用12个月拟议剂量(64mg)Roluperidone的患者数量不足。为了解决这些缺陷,FDA规定Minerva必须至少再提交一项积极、充分和对照良好的研究,以支持Roluperidone治疗阴性症状的安全性和有效性。Minerva还必须提供额外的数据来证明Roluperidone与其它抗精神病药物联合用药的安全性和有效性,以进一步支持Roluperidone的有效性并证明拟议剂量的长期安全性。
总结
FDA在创新药的上市审批上日渐趋严,以高标准、高要求将多款创新药被拒之门外。
FDA的拒批原因主要集中疗效、安全性、CMC问题和标签缺陷上,上市申请被拒除了影响产品的商业化进程外,也可能使企业遭受重大的股市打击,因此企业应审慎考虑FDA审批标准,减少碰壁几率,以期成功闯关FDA。




