肿瘤免疫治疗在肿瘤治疗领域正变得越来越重要,并在治疗各种晚期恶性肿瘤方面显示出良好的效果。然而,耐药性和不良反应仍然是免疫治疗管理的主要挑战。免疫治疗的未来方向是确定新的靶点,开发联合治疗和减少副作用的新方法。
泛素化是一种典型的蛋白质翻译后修饰。在此过程中,泛素与底物共价结合,并介导其转移至26S蛋白酶体复合体进行降解。E3泛素连接酶是泛素化反应中的关键酶,介导泛素-蛋白酶体系统中底物的识别,并确定泛素化反应的特异性。
目前,越来越多的E3连接酶被确定为肿瘤免疫反应的关键调节因子,包括MARCH家族和FBXO38,它们介导程序性细胞死亡受体1(PD-1)的蛋白酶体降解。在肿瘤免疫治疗中,靶向E3连接酶可以增强抗肿瘤免疫。因此,靶向E3连接酶可能是临床肿瘤免疫治疗的有效策略。
泛素化由泛素激活酶(E1)、泛素结合酶(E2)和泛素连接酶(E3)的信号级联催化,并导致泛素与目标蛋白的共价结合。泛素以ATP依赖的方式被激活,并通过硫酯键与E1上的半胱氨酸残基结合。随后,激活的泛素分子转移到E2的半胱氨酸活性位点,然后被招募到E3连接酶中。最后,E3连接酶将E2 Ub复合物与目标蛋白结合,并促进泛素与底物赖氨酸残基的结合。
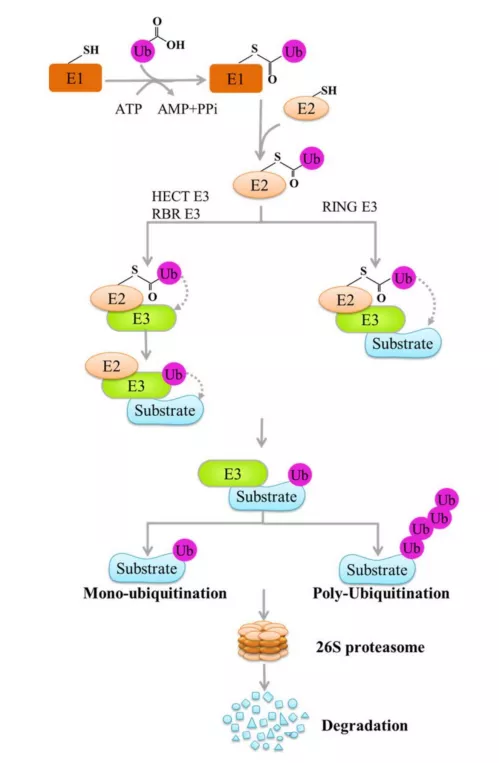
泛素分子不仅可以与七个赖氨酸残基(Lys6、Lys11、Lys27、Lys29、Lys33、Lys48和Lys63)进行单泛素化,还可以基于原始目标底物形成多泛素链。单泛素化是将泛素分子添加到赖氨酸残基上,而多泛素化是在底物上的单个残基上形成泛素链。在多泛素化链中,Lys48-和Lys11-连接的多泛素化与蛋白酶体降解有关,Lys63-连接的多泛素化可参与细胞信号组装和转导。泛素化与各种生物过程密切相关,包括内化和溶酶体靶向、蛋白质相互作用调节、亚细胞分布变化、转录调节、生长反应、先天免疫反应、DNA修复和复制以及跨膜信号转导,尤其是在核因子-κB(NF-κB)途径的调节。
E3泛素连接酶根据其结构特征和作用机制,可以被分为三个家族:RING E3s、HECT E3s和RBR E3s。E3连接酶结合E2 Ub复合物和底物后,RING E3s催化泛素从E2直接转移到底物的赖氨酸残基,而HECT和RBR E3连接酶催化泛素从E2转移到半胱氨酸,半胱氨酸是E3连接酶的活性部位,随后泛素转移到底物蛋白。E3连接酶在人类癌症的发生和发展中起着至关重要的作用。
PD-1/ PD-L1
PD-1/ PD-L1信号通路在逃避免疫监视的肿瘤中起着至关重要的作用。Lys48连接的多泛素化修饰是PD-1翻译后的第一个蛋白质修饰,可以调节活化T细胞表面的PD-1蛋白水平和抗肿瘤免疫。FBXO38是一种多蛋白复合物,是PD-1的一种特异性E3连接酶。它介导PD-1的蛋白酶体降解,从而下调表面PD-1表达并阻断PD-1/PD-L1介导的肿瘤免疫逃逸,这使FBXO38成为抗肿瘤免疫剂开发的潜在靶点。
单泛素化和多泛素化均可以调节PD-L1的表达、膜位置和功能。PD-L1的免疫抑制活性受到泛素化和N-糖基化的严格调控。糖基化后,PD-L1转移到细胞表面,而非糖基化的PD-L1通过糖原合成酶激酶3β(GSK3β)磷酸化,触发它与Cullin-RINGE3连接酶配体蛋白β-TrCP的相互作用,从而促进PD-L1多泛素化和随后的蛋白酶体依赖性降解。
这些研究表明,E3连接酶对PD-1/PD-L1降解至关重要,靶向E3连接酶可使癌症患者对肿瘤ICB治疗感,并提高免疫治疗的疗效。
CTLA4/B7
参与CTLA-4蛋白降解的E3连接酶仍然未知,初步证据表明CTLA-4蛋白丰度与E3连接酶之间存在潜在关系。MARCH蛋白是RING E3连接酶的一个亚家族,是免疫反应的关键调节因子。MIR2,一种新型膜结合E3连接酶,可通过诱导B细胞内吞作用降解CD86,导致免疫逃逸。此外,MIR2泛素化CD86并诱导CD86被内吞以降解免疫细胞。
最近的一项研究报告,MARCH1上调与CD86表达呈负相关。MARCH1 E3连接酶介导DC中CD86的泛素化和降解,这对于调节DC的抗原呈递至关重要。此外,MARCH8介导CD86在其C末端的多泛素化,导致其快速内吞和溶酶体依赖性降解。
LAG-3/ MHC-II
MHC-II的表面表达和半衰期由泛素化控制。MARCH E3连接酶家族,包括MARCH1和MARCH8,被认为可以抑制MHC-II的表达。两种MARCH都通过泛素化MHC-IIβ链的细胞质尾部来调节肽MHC II复合物。MARCH8泛素化MHC-IIIAβ链225位的赖氨酸残基,并下调细胞表面MHC-II分子的表达,从而抑制T细胞的激活和功能。此外,MARCH1介导DC表面MHC-II分子的泛素化,这种泛素化诱导MHC-II的内吞和降解,从而抑制抗原呈递并促使肿瘤细胞逃避免疫破坏。
然而,目前对LAG-3蛋白调节的理解仍然有限,尤其是其翻译后泛素化修饰。
KIR/MHC-I
KSHV的K1基因产物,如MIR1和MIR2,是E3连接酶,可以通过赖氨酸-63连接的多泛素链降解MHC-I分子。此外,US2/TRC8复合物和TMEM129 E3连接酶也介导MHC-I分子的泛素化和降解。
一些MARCH蛋白下调MHC-I分子的细胞表面表达,例如,由MARCH1介导的MHC-II泛素化降低表面MHC-I表达并影响MHC-I抗原呈递。MARCH4和MARCH9直接介导MHC-I分子的泛素化,导致其内吞和溶酶体降解。
TIM-3
TIM-3促进或抑制细胞免疫反应的具体机制取决于所涉及的配体和细胞环境。虽然降解TIM-3及其配体的确切E3连接酶尚未发现,但E3连接酶与TIM-3及其配体之间的潜在关系可能会影响肿瘤免疫。已经发现,TIM-3配体之一PtdSer的转运受泛素化调节,泛素化由MET30基因编码的SCF泛素连接酶复合物介导。
TIGIT及其配体CD155和CD112
TRC8(RNF139)E3连接酶可以识别并有效降解CD112,抑制CD112泛素化可以增加其在肿瘤细胞表面表达,从而提高肿瘤细胞对NK细胞毒性的敏感性,增强NK细胞对肿瘤细胞的杀伤作用。此外,由于缺乏对TIGIT及其配体的最新研究,它们与E3连接酶之间的确切关系尚不清楚。
CD47/ SIRPα
Cullin-RING连接酶4(CRL4)是E3连接酶家族的成员,该家族由RBX1、CUL4支架蛋白和DDB1-CUL4相关底物受体组成。CD47被DDB1-CUL4A泛素化,然后运输到蛋白酶体降解,从而阻断CD47/SIRPα信号通路并增强抗肿瘤免疫。
NF-κB信号通路
NF-κB通路与肿瘤免疫密切相关,可通过靶向E3连接酶精确调节。E3连接酶参与NF-κB信号激活的三个步骤:NF-κB抑制剂IκB的降解、NF-κB前体的处理以及通过非降解机制激活IκB激酶(IKK)复合物。
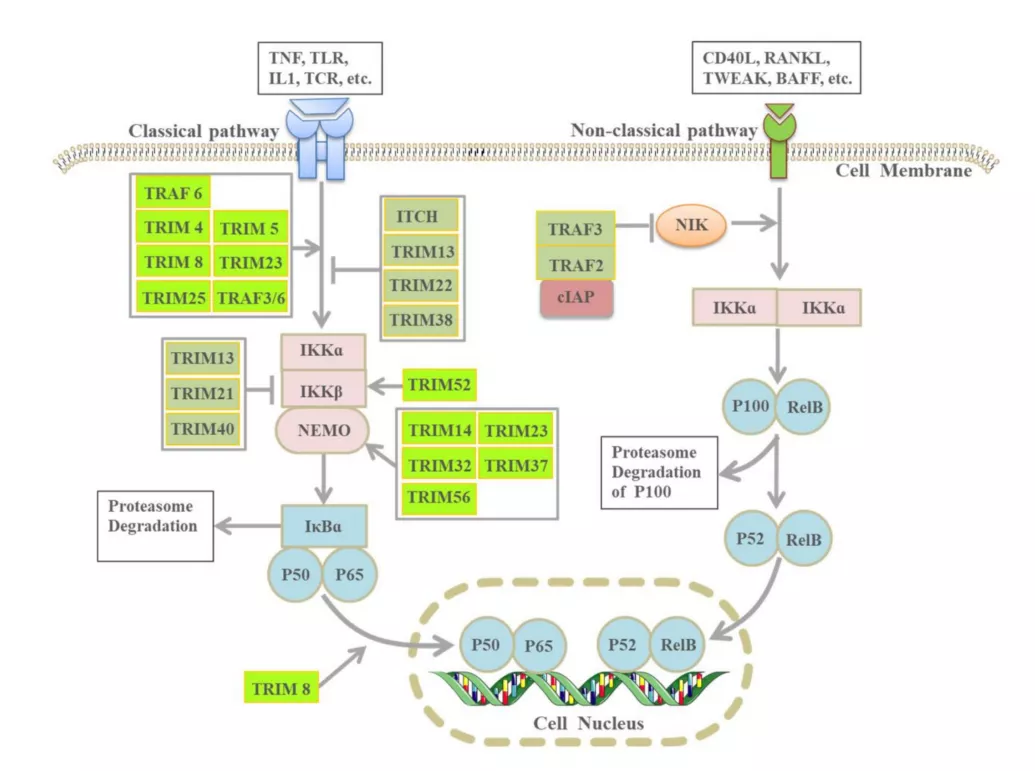
TNF受体相关因子(TRAF)是一个信号分子家族,在先天性和适应性免疫细胞生物学中起着关键作用。除了缺乏RING结构域的TRAF1外,所有TRAF都具有E3连接酶活性。TRAF家族成员可以积极或消极调节经典和非经典NF-κB信号。
TRAF6激活IL-1并与TLR介导的NF-κB通路激活相关,而TRAF2/5与TNFR1介导的NF-κB通路激活相关。此外,TRAF2和TRAF3是非经典NF-κB途径的关键负调节因子。在正常生理条件下,NF-κB诱导的激酶(NIKs)通常与TRAF3结合。TRAF–cIAP E3连接酶复合物由TRAF2、TRAF3和细胞凋亡抑制剂(cIAPs)组成,可与NIKs结合并通过TRAF3蛋白降解NIKs,从而防止NIKs累积和激活非标准NF-κB信号。当接收到诸如CD40L、BAFF和RANKL等通路激活信号时,TRAF2和cIAP1/2介导TRAF3的降解,然后释放NIKs,从而导致非常规NF-κB激活。
三元基序(TRIM)是一种典型的E3连接酶,是一个参与NF-κB信号通路的泛素依赖性蛋白水解的多成员家族。TRIM4、5、8、14、23、25、32、37、52和56稳定增加NF-κB活性,而TRIM13、21、22、38和40抑制NF-κB活性。
JAK-STAT信号通路
JAK-STAT信号通路是肿瘤发生、发展和免疫逃逸的关键通路。JAK-STAT途径由三种类型的负调节因子组成:磷酸酶(SHPs、CD45和PTP1B/TC-PTP)、细胞因子信号抑制剂(SOCS)蛋白和活化STAT蛋白抑制剂(PIAS)。SOCS蛋白表现出E3连接酶的活性,导致信号分子(包括细胞因子受体和JAK激酶)的蛋白酶体降解。SOCS1基因沉默增强DC的抗原提呈和抗肿瘤免疫。
PIAS蛋白可与E2连接酶Ubc9结合,并通过RING指结构域进行SUMO修饰以显示E3连接酶活性,导致目标蛋白STAT二聚体降解并抑制JAK-STAT的激活。PIAS3是STAT3的特异性抑制剂。因此,增强或抑制这些负性调节蛋白的作用可以阻断JAK-STAT信号介导的肿瘤免疫细胞逃逸,提高肿瘤免疫治疗的疗效。
STING信号通路
干扰素基因刺激因子(STING)是一种位于内质网内的跨膜适配蛋白,是检测肿瘤的重要天然免疫传感器。APC中STING通路的激活导致IFN-β的产生和CD8+T细胞的诱导,从而启动并激活适应性抗肿瘤免疫反应。
目前,在STING途径中发现了多种多泛素化,包括K63、K48、K11和K27的多泛素化。E3连接酶Trim56和Trim32通过催化STING的K63连接的多泛素化增加STING介导的IFN-β表达。两项研究也证实Trim29是STING的E3连接酶。其中一项研究发现,使用Trim29降解气道上皮细胞和髓系树突状细胞中的STING可减少I型干扰素的产生,这有助于EB病毒(EBV)在两种细胞类型中建立持续感染。
E3连接酶在肿瘤免疫中起着至关重要的作用,E3连接酶的药物开发是近年来极具挑战性的研究热点。目前,针对E3连接酶的抗肿瘤药物根据其作用机制主要分为四类:E3连接酶的靶向抑制剂、E3连接酶的靶向激动剂、蛋白水解靶向嵌合体(PROTAC)和分子胶。
E3连接酶抑制剂
目前,越来越多的E3连接酶抑制剂已被开发并用于临床试验。近年来开发的RING E3连接酶抑制剂主要是针对CRL的小分子抑制剂。许多RING E3连接酶抑制剂在癌症免疫治疗或联合治疗的临床前模型和临床试验中显示出相当大的治疗潜力,其中研究最多的抑制剂包括IAP家族、MDM2、pVHL、Skp2和β-TrCP。
IAP拮抗剂在促进抗肿瘤免疫方面起着至关重要的作用。IAP拮抗剂,如LCL161,诱导多发性骨髓瘤中肿瘤细胞的TNF依赖性凋亡,并促进抗肿瘤免疫,在晚期实体瘤患者的1期临床试验(NCT01098838)中显示出高度的安全性和有效性。目前,一些关于IAP拮抗剂和其他抗癌药物协同作用的研究正在进行I/II期临床试验(NCT02649673、NCT04643405)。
MDM2抑制剂通过抑制MDM2的E3连接酶活性和干扰MDM2-p53相互作用发挥作用。许多具有独特结构、高效的MDM2抑制剂已经进入临床阶段,包括RG7112(RO5045337)、SAR405838(MI-77301)和idasanutlin(RG7388)。然而,p53突变引起的剂量限制毒性和耐药性是临床试验中的两大挑战。
与RING E3连接酶相比,对HECTE3连接酶抑制剂和RBR E3连接酶抑制剂的研究很少。一些研究中的分子大多处于临床前阶段。
E3连接酶激动剂
除了E3连接酶抑制剂外,还发现一些E3连接酶激动剂可促进抗肿瘤免疫。
CRBN(cereblon)是CRL4CRBN E3连接酶复合物的底物识别亚单位。Thalidomide及其衍生物lenalidomide和pomalidomide是CRL激动剂的代表药物,主要靶向CRBN蛋白。它们与CRBN结合并改变CRBN E3连接酶复合物的底物特异性,导致下游蛋白质泛素化和降解,并刺激T细胞活化。它们广泛用于淋巴瘤和骨髓瘤的临床治疗。CC-90009是一种新发现的cereblon E3连接酶调节剂,CC-90009联合CRL4CRBN可选择性靶向GSPT1进行泛素化和蛋白酶体降解,可用于治疗急性髓系白血病。
β-TrCP是E3连接酶,负责非糖基化PD-L1的多泛素化和降解。Resveratrol是一种E3连接酶调节剂,调节PD-L1泛素化。它通过靶向β-TrCP E3连接酶诱导非糖基化PD-L1多泛素化,从而降低PD-L1在三阴性乳腺癌细胞中的表达并增强抗肿瘤免疫。此外,一项研究设计了各种小分子,可增强SCFβ-TrCP和致癌转录因子β-catenin之间的相互作用,包括NRX-252114和NRX-252262。这些化合物揭示了增强E3连接酶-底物相互作用以靶向某些致癌蛋白质降解的可行性。
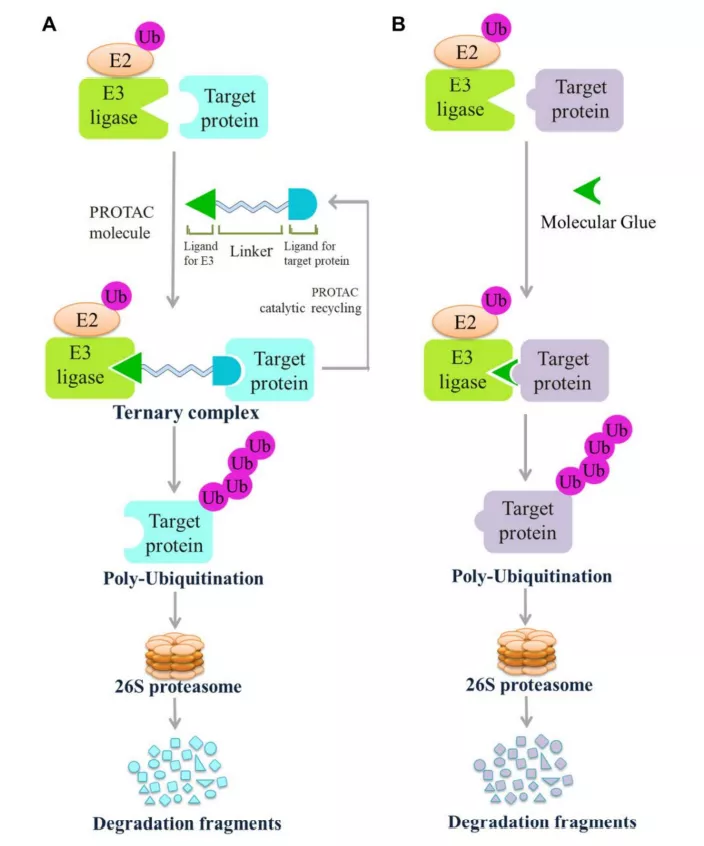
PROTACs
目前,基于E3连接酶的PROTACs已成为抗癌药物研究领域的热点。第一个进入临床试验的PROTAC药物Arvinas开发的ARV-110,一种针对雄激素受体的口服小分子,它于2019年进入了治疗转移性去势抵抗前列腺癌的1期临床试验(NCT03888612)。此外,Arvinas开发了用于治疗乳腺癌的PROTAC药物ARV-471。ARV-471是一种针对雌激素受体的降解剂,已进入2期临床试验(NCT04072952)。
BET蛋白家族,包括BRD2、BRD3和BRD4,在癌症中起着重要作用,其中BRD4蛋白参与调节癌症和炎症过程。研究人员发现,PROTAC分子MZ1可以形成BRD4-MZ1-VHL三元复合物,它可以介导BRD2、BRD3和BRD4蛋白质的降解。基于MZ1的晶体结构,开发了AT1,它可以专门针对BRD4降解。此外,其他研究已经开发出名为MT1的二价蛋白质,它可以结合两种BRD4蛋白质,并具有更有效的降解BRD4蛋白质的能力。最近,三价PROTAC SIM1被设计成具有更高的降解效率和更强的抗癌活性。
分子胶
分子胶降解剂在E3连接酶和目标蛋白之间诱导新的相互作用,从而降解目标蛋白。诱导靶蛋白水解的分子胶包括免疫抑制剂环孢素A(CsA)、FK506和thalidomide。与传统的小分子酶抑制剂或受体拮抗剂相比,分子胶最显著的优点是它不需要在靶蛋白上存在与活性相关的口袋。因此,它可以降解无配体的蛋白质。
分子胶可促进约600个E3连接酶与20000多个潜在靶蛋白之间的相互作用,从而为探索新靶点和潜在小分子药物提供了方向。Asukamycin是manumycin聚酮类化合物的成员,作为UBR7和p53之间的分子粘合剂,靶向E3连接酶UBR7和乳腺癌细胞中的肿瘤抑制因子p53之间的相互作用,导致p53转录激活和细胞死亡。
Thalidomide及其衍生物lenalidomide和pomalidomide具有免疫调节特性,他们可以招募锌指转录因子和靶蛋白到CRBN,导致其泛素化和降解。通过结合CRL4-CRBN降解蛋白质的其他分子胶包括CC-885、CC-90009、CC-92480、CC-220和CC-122。其中CC-90009(NCT02848001、NCT04336982)和CC-92480(NCT03989414)已进入临床试验。
此外,一些已进入临床试验的分子胶包括DKY709(NCT03891953)、CFT7455(NCT04756726)和BTX-1188。DKY709作为单一药物并与PD-1拮抗剂联合用于实体瘤的I期临床试验。CFT7455作为口服药物用于复发或难治性非霍奇金淋巴瘤或多发性骨髓瘤的I/II期临床试验。
由于泛素化参与调节肿瘤免疫的多个过程,E3泛素连接酶可能是联合肿瘤免疫治疗的潜在治疗靶点,靶向E3泛素连接酶在肿瘤免疫治疗中表现出巨大的潜力。
然而,考虑到人体内由泛素化调节的复杂而广泛的生命活动,阻断或激活E3连接酶治疗肿瘤可能对其他正常生命代谢活动产生不利影响。因此,探索和解决这一问题仍然是一个相当大的挑战。此外,选择合适的治疗窗口来使用E3连接酶抑制剂或激动剂仍需要进一步探索。相信随着研究的深入和临床的进展,这些问题都可以得到解决,靶向E3泛素连接酶将在肿瘤免疫治疗中展现出良好的应用前景。
参考文献:
1.Potential of E3 Ubiquitin Ligases in CancerImmunity: Opportunities and Challenges. Cells. 2021 Dec; 10(12): 3309.
本文摘自---药精通 Bio
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 南京市江宁区科学园乾德路5号