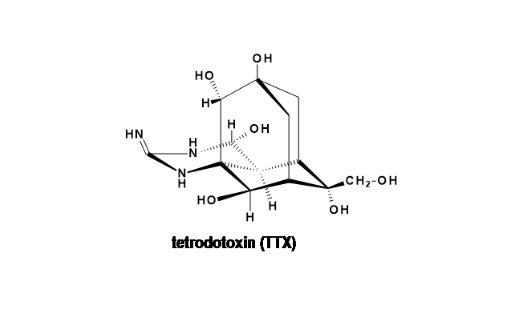
河豚鱼(pufferfish, puffers),你可能并不陌生,因为媒体上经常能够看到误食河豚鱼引起食物中毒和死亡的案例。其种类多样,分布在我国黄海、渤海及东海区域。河豚是一种名贵的高档水产品,肉味鲜美、营养丰富。但河豚鱼的脏器特别是肝脏、卵巢、和血液中含有剧毒物质,如果处理不当或误食,轻者中毒,重者丧命。这种剧毒物质是一种化学结构叫做河豚毒素的分子。
人们攝入微克级的河豚毒素就可能中毒,约1~2毫克河豚毒素便可致命。误食河豚鱼有毒部分后,其中毒症狀通常会在约30分钟出現,但亦可在2-3小时出现。中毒症狀有上腹部不适,恶心、呕吐、腹痛、继而口唇舌尖及肢体麻木、全身麻木,舌头发硬,语言障碍,面色潮红,上睑下垂,瞳孔缩小,全身麻痹瘫痪,不能行走,重者有呼吸急速等呼吸症狀,直至呼吸麻痹而死亡。
河豚毒素(Tetrodotoxin, TTX)是一种非肽类的胍类神经毒素,主要存在于河豚和其他海洋生物中。它的化学结构稳定,在加热和盐腌制河豚鱼的过程中均不能被破坏。
它的化学结构如上图,乍看上去就像一个鸟笼,有几个类似葡萄糖的结构,含有一个胍基,所以,不难理解它是胍类的神经毒素。强调它是非肽类的神经毒素,是为了区分肽类神经毒素。因为许多神经毒素都是小分子的肽类化合物,如来自于芋螺(Cone snail)的神经毒素就含有千千万万个分子结构各异的肽类化合物;蜘蛛毒液、蜜蜂的蜂毒(bees)、蝎子毒素(scorpions)、蛇毒和海葵(sea anemones)毒素等大多是肽类的毒素为主。所以,从化学结构上说,河豚毒素就很特别。
河豚毒素通过阻断电压门控钠通道 (voltage-gated sodium channel,VGSC)导致麻木、呼吸麻痹等症状。什么是电压门控钠通道?我们知道有一种叫电鳗的鱼,主要生活在南美洲亚马孙河流域,多在浅水的池沼或水体较混浊的岸边活动。这种电鳗可以放电,能够产生足以将人击昏的电流,输出的电压可达300~800伏。电鳗的放电来自于它特化的肌肉组织所构成的放电体。肌肉组织几乎都能放电,占其身长的80%以上,有数以千计的放电体。每个放电体都相当于一个发电机,这个放电体的发电机就是由电压门控钠通道组成。河豚毒素能够阻断这个电压门控钠通道。
河豚毒素通过阻断电压门控钠通道来产生麻木和呼吸麻痹的毒性。电压门控钠通道是一种膜蛋白,也是发动神经脉冲动作电位的第一个蛋白。河豚毒素和钠通道的site-1位点结合, 通过结合于电压门控钠通道(VGSCs)的site-1位点来阻断钠通道的打开,因此,阻断了神经脉冲的产生和传递。神经脉冲的产生和传递被阻断了,就产生了麻痹、麻醉的作用,因此,河豚毒素除产生致命性的副作用外,河豚毒素本身是非常强的局部麻醉剂,同时也具有很好的神经镇痛的作用。
天然河豚毒素经皮下或肌肉注射具有非常强的麻醉作用。在河豚毒素的麻醉作用方面,研究最多的是哈佛大学麻醉系的Daniel S. Kohane教授。 行为学药理实验表明,河豚毒素具有强烈神经阻断作用,通过结合于TTX-敏感的钠通道特别是钠通道亚型Nav1.7,阻断动作电位的产生。
电压-门控钠通道(voltage-gated sodium channels)参与神经病理性疼痛的发生和发展。按照钠通道对河豚毒素的敏感性的不同可以将钠通道分河豚毒素-敏感型(TTX-sensitive)钠通道和河豚毒素-抵抗型(TTX-resistant,TTX-R)钠通道。TTX-sensitive钠通道包括Nav1.3, Nav1.4, Nav1.6, Nav1.2, Nav1.1和Nav1.7亚型;TTX-resistant钠通道有钠通道亚型Nav1.5, Nav1.8, 和 Nav1.9。在生理状态下钠通道亚型Nav1.1, Nav1.6, Nav1.7, Nav1.8, Nav1.9主要分布在外周神经(PNS) 。然而,在病变状态下,如在多种动物疼痛模型中,Nav1.3和 Nav1.6钠通道亚型在外周神经上表达大大增加,因此,TTX-sensitive钠通道亚型Nav1.1, Nav1.3,Nav1.6, Nav1.7和神经痛的发生和发展密切相关。TTX-resistant钠通道亚型中,Nav1.8 与外周神经痛密切相关。
TTX-sensitive钠通道亚型参与神经病理性疼痛的另一个重要证据来自于钠通道亚型Nav1.7基因突变的发现。在三个有血缘关系的家庭中,其NaV1.7上功能丢失基因突变(loss-of-function mutations)导致其家庭成员感知疼痛的能力完全缺失。这种被称作通道病相关的疼痛缺失(channelopathy-associated insensitivity to pain)表明钠通道亚型NaV1.7和神经痛的相关程度极高。自此,作用于钠通道亚型Nav1.7拮抗剂成为发现新的抗神经痛药物的希望所在,许多制药公司和新药研发公司开始了寻找选择性作用于钠通道亚型Nav1.7拮抗剂的竞赛。然而,令人遗憾的是,经过了10多年的努力,至今仍没有一个Nav1.7拮抗剂被FDA批准上市。
河豚毒素是来源于天然的小分子化合物,属于强效site-1钠通道阻断剂。通过结合于神经细胞膜表面的电压-门控钠通道和干扰神经疼痛信号传递,发挥其阻断或减轻疼痛的作用。河豚毒素对外周神经系统有特异性作用,对中枢神经系统没有作用,也没有成瘾性。
和选择性作用于Nav1.7拮抗剂不同,河豚毒素作用于TTX-敏感的所有钠通道亚型。除作用于在外周神经大量表达的Nav1.7亚型外,河豚毒素还作用于在神经病变状态下大量表达的钠通道亚型Nav1.3和神经病变状态下表达增加的钠通道亚型Nav1.6。
作为广泛作用于外周神经上TTX-敏感的所有钠通道亚型,河豚毒素目前正处于临床III期的药物试验阶段。被称作Halneuron™ (injectable Tetrodotoxin,TTX,河豚毒素)的试验药物,由WEX Pharmaceuticals Inc.研制。Halneuron被认为是更安全、等效或优于阿片类镇痛效果的非阿片类镇痛剂。主要用于肿瘤化疗引起的神经痛以及肿瘤相关的疼痛。对于肿瘤痛适应症,河豚毒素已经完成了两个III期临床试验(临床ID:NCT00725114 和 NCT00726011);对于肿瘤化疗-引起的神经痛适应症,河豚毒素已经完成了一个II期临床试验(临床ID:NCT01655823),进一步的双盲、多中心临床试验正在招募中(于2022年5月公布)。新的临床ID是NCT05359133,招募对象是(顺)铂类化疗和紫杉醇类化疗-诱导的中等到严重的神经痛患者。抗神经痛药物河豚毒素研发的改进(me-better)
目前,WEX公司在河豚毒素的临床研究走在最前面, 并且有专利保护。科学家们对河豚毒素做了大量的基础研究,也一直在努力提高河豚毒素的疗效和降低河豚毒素的系统性毒性。哈佛大学麻醉系的Daniel S. Kohane 教授研究组长期专注site1钠通道阻断剂的研究。主要采用剂型改造如脂质体包裹、缓释等方法研发新的长效局麻药和神经镇痛药,目标是提高site-1钠通道阻断剂在临床上的镇痛效果同时降低其系统性毒性。该研究组发表了大量有关site-1钠通道阻断剂文章。但脂质体包裹等方法有它的缺点,如脂质体本身能够引起炎症,诱导神经痛。
我们在Wex公司和哈佛大学的研究的基础上,一直不懈地做些相关的工作,发现了一种通过结构改造的方法延长河豚毒素的作用时间。该项目旨在基于河豚毒素的构效关系、分子药理学和药代动力学的作用特性,通过全新设计和合成新型site-1钠通道阻断剂,开发新的长效神经镇痛药和长效局麻药。后续的研究正在进行中。