格氏试剂可与醛、酮反应形成醇,它们和碳与杂原子形成的双键之间的反应称为格氏反应。
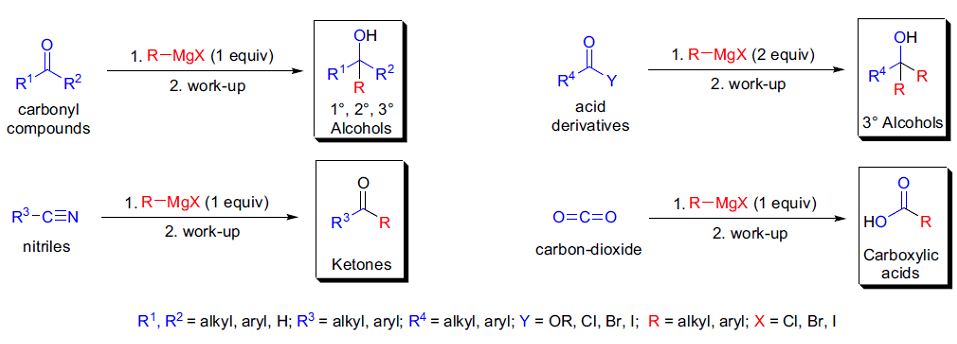
反应机理
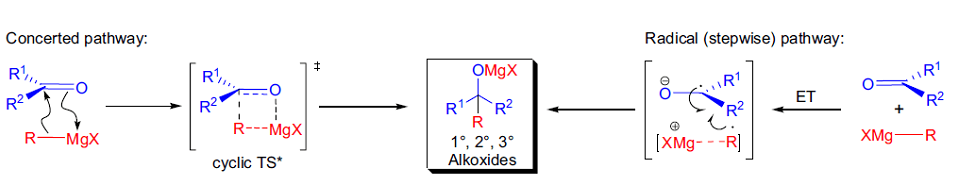
关于格氏试剂的形成机理很可能是单电子的迁移过程,它主要发生在金属的表面。有人认为它可能是通过一个concerted过程或是一个radical途径。
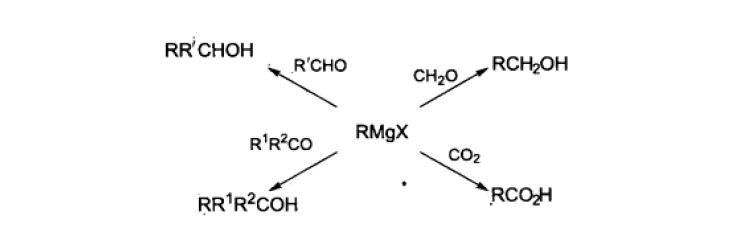
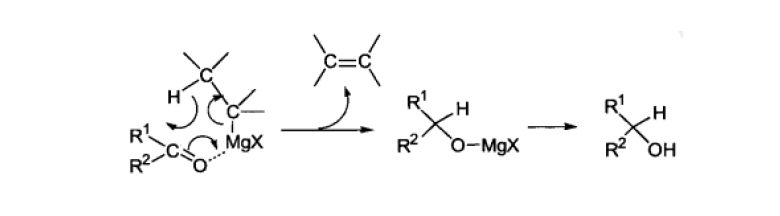
格氏试剂的最重要用途是与羰基化合物反应。与醛、酮反应分别得到仲醇和叔醇。与二氧化碳反应则得到羧酸。
当酮或格氏试剂的位阻大时,可能发生两个副反应:去质子化和还原反应。格氏试剂与含α-H的酮可能发生质子化产生烯醇负离子,水解后重新生成原料酮,此时格氏试剂作为碱。
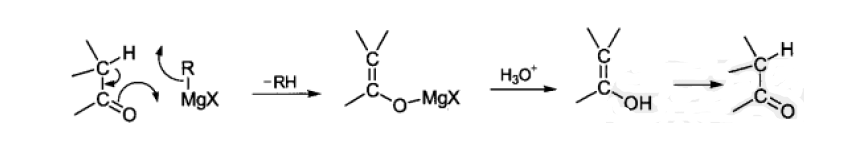
含β-H的格氏试剂与酮可能发生类似于Meerwein-Ponndorf-Verley还原的副反应。反应经过六元环过渡态。
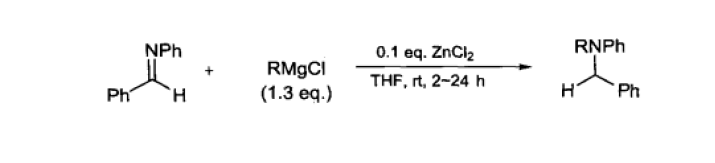
亚胺的活性比羰基低,但在Lewis酸存在下,或通过亚胺鎓盐形式,格氏试剂可与之加成。
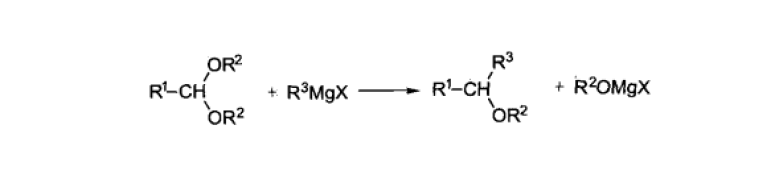
缩醛对格氏试剂有一定稳定性,但是在激烈条件下,可发生烷氧基被取代的反应。
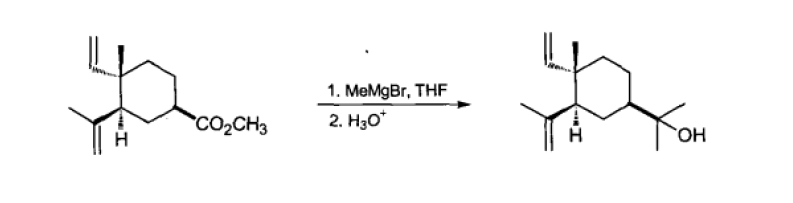
格氏试剂与羧酸酯、内酯或酰氯反应难以停留在酮,而是直接生成叔醇,可用于含两个相同烷基的叔醇的制备。
格氏试剂与N-甲氧基-N-甲基酰胺加成是合成酮的可靠方法。
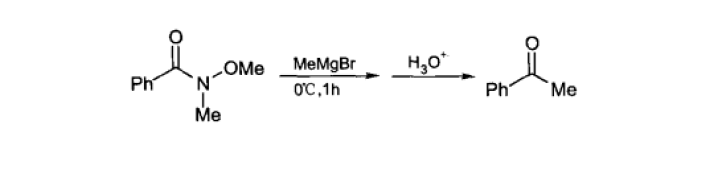
格氏试剂与原酸酯反应可用于醛的制备。与酰亚胺反应得氮杂半缩醛。
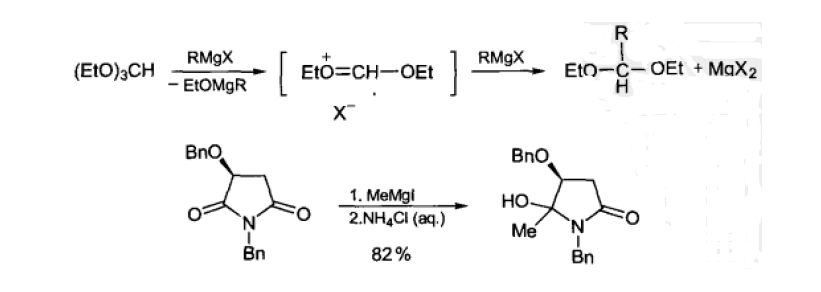
参考文献
1. Grignard, V. C.R.Acad.Sci. 1900, 1322-1324.
2. Grignard, V. Ann.Chim. 1901, 7, 433-490.
3. Kharasch, M. S., Reinmuth, O. Grignard Reactions of Nonmetallic Substances (Prentice-Hall, New York, 1954) 1267 pp.
4. Shirley, D. A. T Org. React.1954, 8, 28-58.
5. Sun, P., Sun, C., Weinreb, S. M. J. Org. Chem. 2002, 67, 4337-4345.
6. White, J. D., Shin, H., Kim, T.-S., Cutshall, N. S. J. Am. Chem. Soc. 1997, 119, 2404-2419.
7. Kuehne, M. E., Xu, F. J. Org. Chem. 1998, 63, 9434-9439.
8. Taunton, J., Collins, J. L., Schreiber, S. L. J. Am. Chem. Soc. 1996, 118, 10412-10422.
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 南京市江宁区科学园乾德路5号