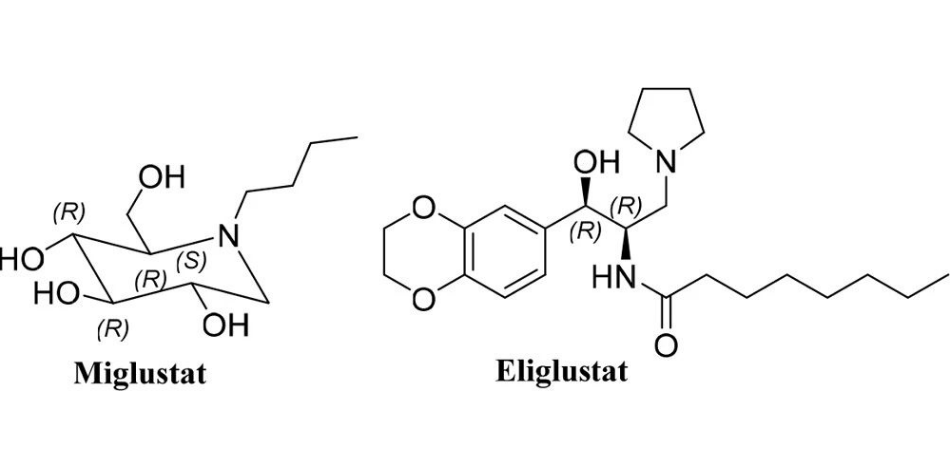
戈谢病(GD),为罕见的常染色体隐性遗传病,也是家族性糖脂代谢性疾病,常用的治疗方法是底物减少疗法 (SRT) 和酶替代疗法 (ERT) 。伊米苷酶(1991年批准)、维拉苷酶(2010年批准)和 taliglucerase alfa (Elelyso)(2012年批准)是三种类型的药物。另外,miglustat是 2002年批准的第一个口服药物。在 2014 年,eliglustat (Cerdelga)已被证明可用于治疗GD1。
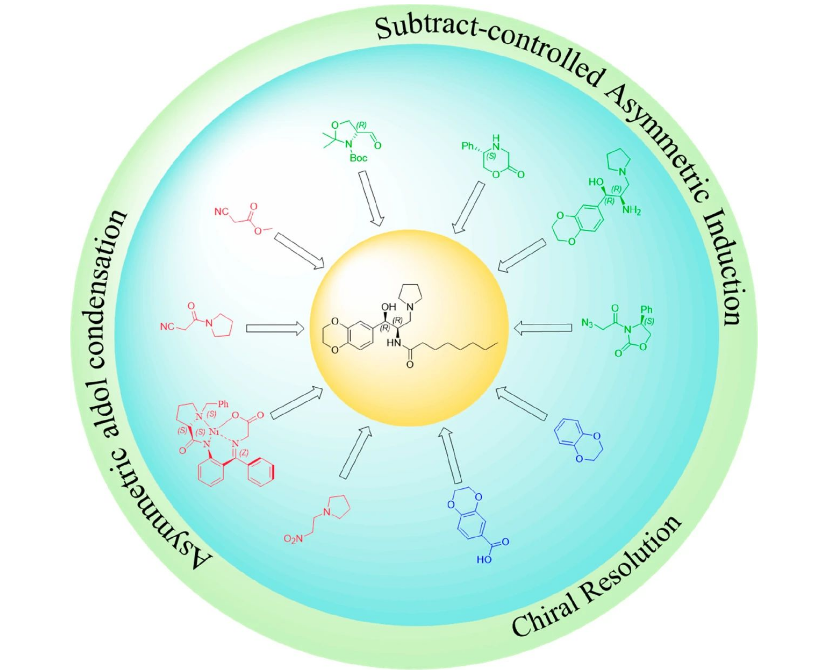
eliglustat 的手性合成方法包括手性拆分,不对称羟醛缩合和手性池合成。
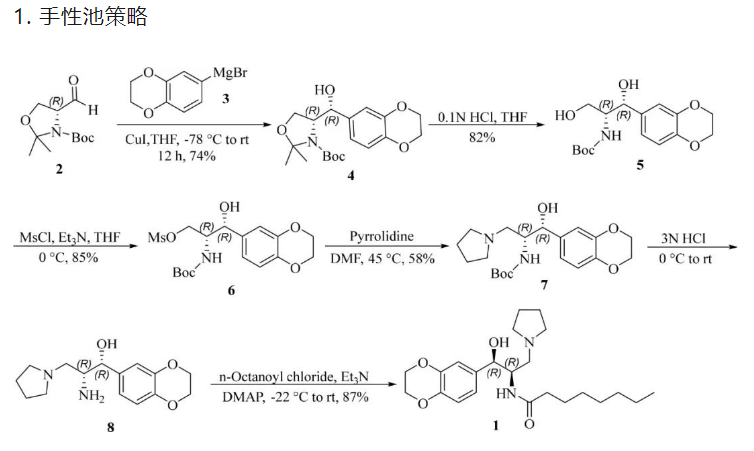
缺点:
1)需要-78 ℃;
2)原料2较贵;
3)制备格氏试剂 3,是高度放热、不易受控的反应,增大生产安全风险。同时,3需要柱色谱纯化。
2. 不对称羟醛缩合
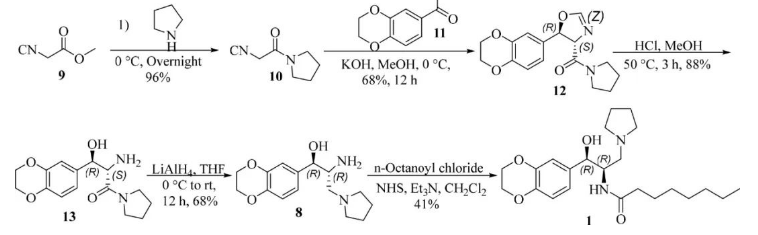
缺点:每个中间体都需要柱色谱纯化。中间体8具有胺基和羟基,会生成酰胺和酯副产物,纯化过程更加困难。该方法在工业上不可行。
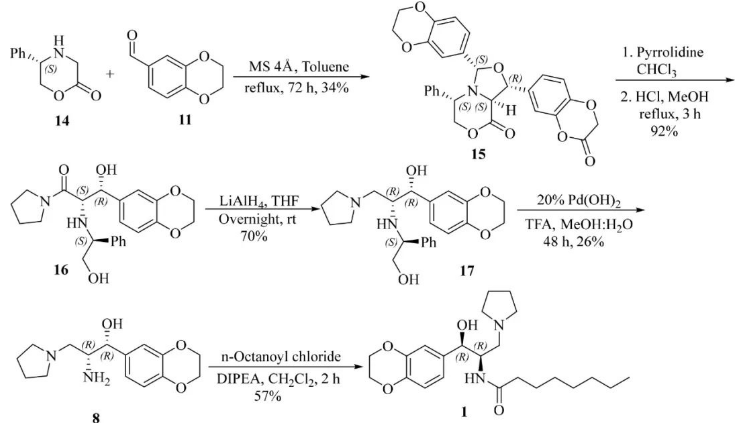
缺点:
1)15的合成时间长、收率低。长时间加热会产生杂质,这对产物 1 的总收率有直接影响。
2)用20% Pd(OH)2 对胺进行脱保护,这提高了合成的总成本。产量,同时降低了化合物8的收率。
3)化合物8含有羟基和胺官能团,在与辛酰氯的反应中相互竞争,生成的这两种产物是结晶点几乎相同的固体,导致纯化困难。
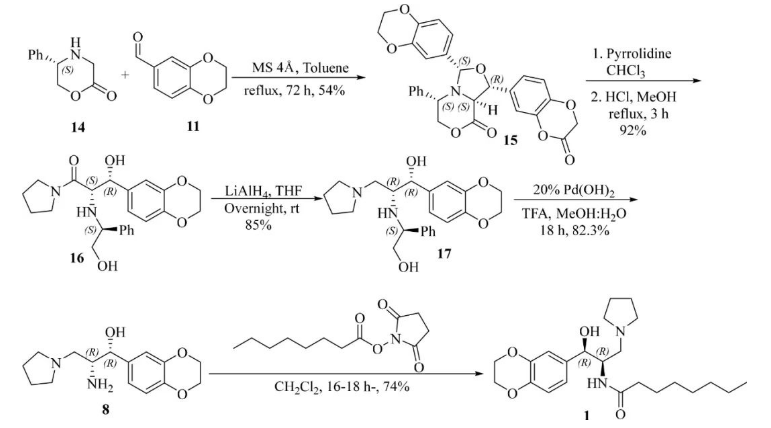
优点:改进了纯化工艺,在不使用色谱纯化的情况下提高了最终产品的收率。
缺点:原料成本高,反应时间较长,收率中等。
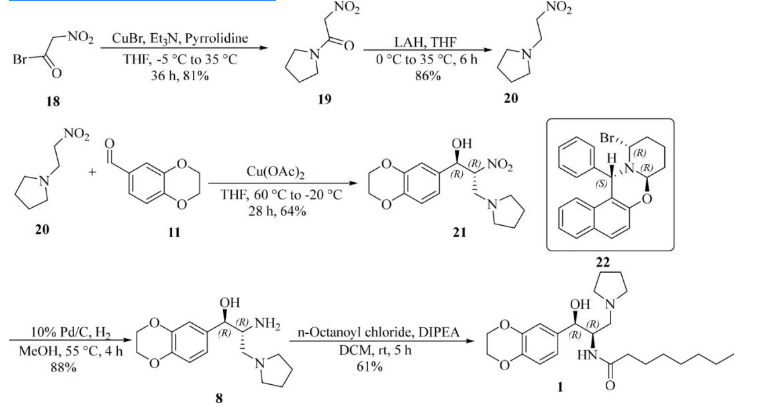
手性配体催化不对称亨利反应
缺点:昂贵的手性催化剂,1同时含有难以分离的辛酰氯的酰胺和酯,因此难以纯化,不适合工业化生产。
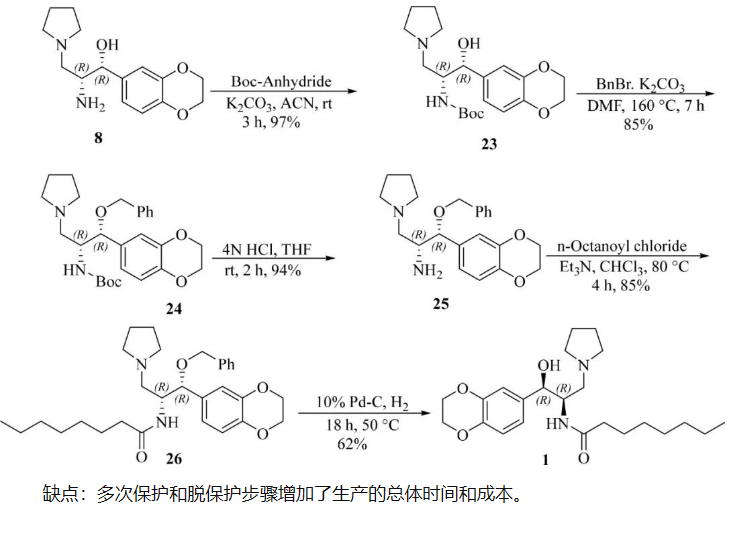
7. 基于手性基团的合成
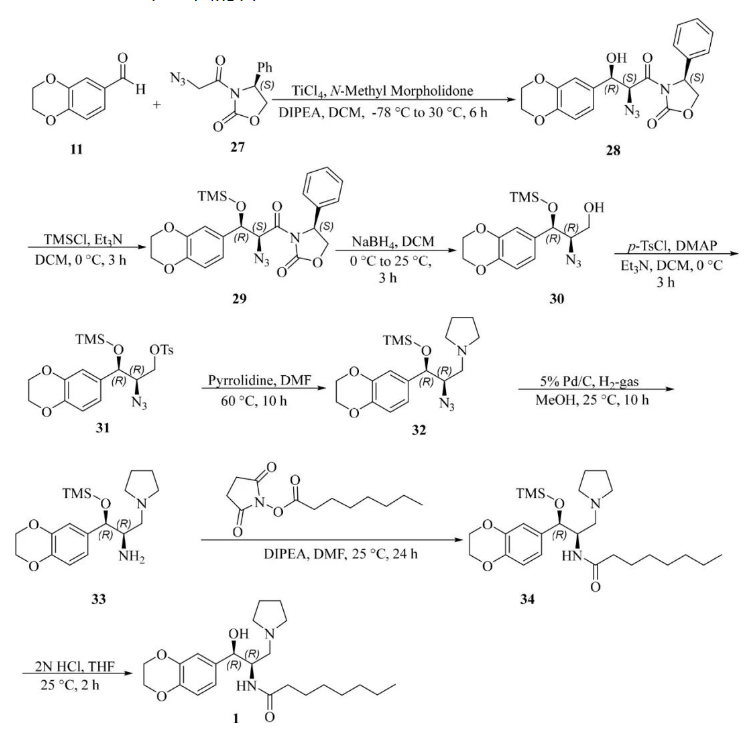
缺点:-78°C的温度;叠氮基化合物32还原步骤,在纯度和产品稳定性方面挑战较大。
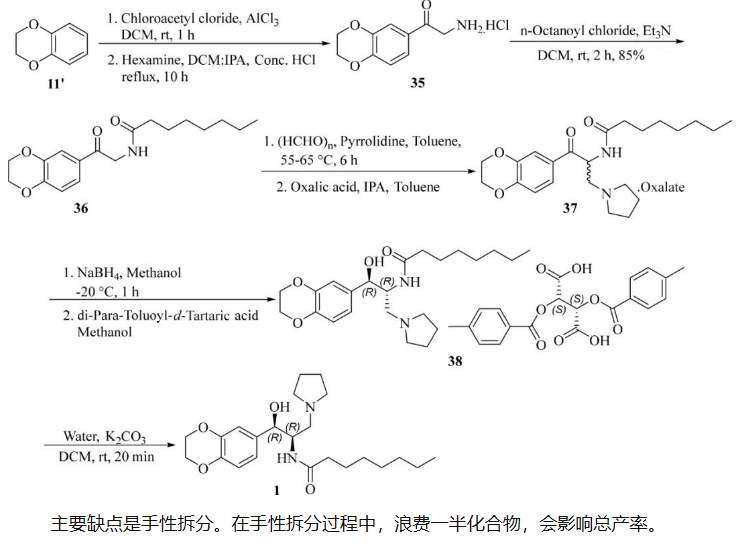
9. 新的合成策略
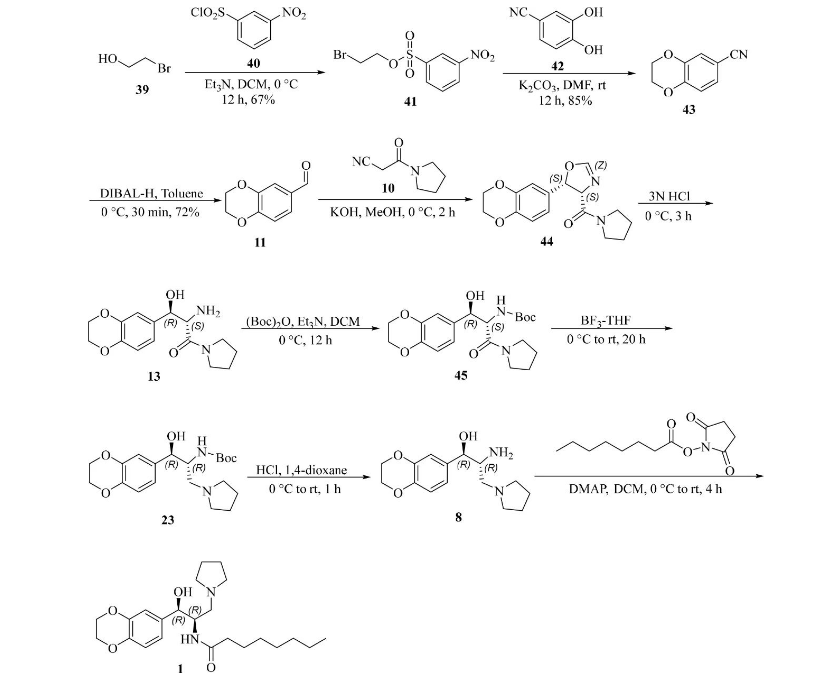
立体选择性分子内环化
该方法中使用的所有起始材料和试剂都很便宜,该合成方法可用于大规模工业生产
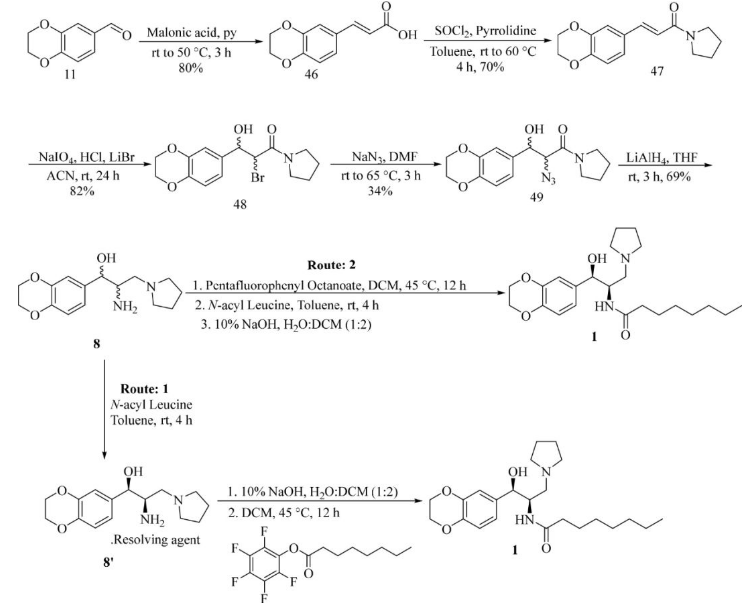
路线1和2中使用的手性拆分步骤降低了化合物1的总产率并增加了生产成本。因此,该方法不适合大规模工业生产。
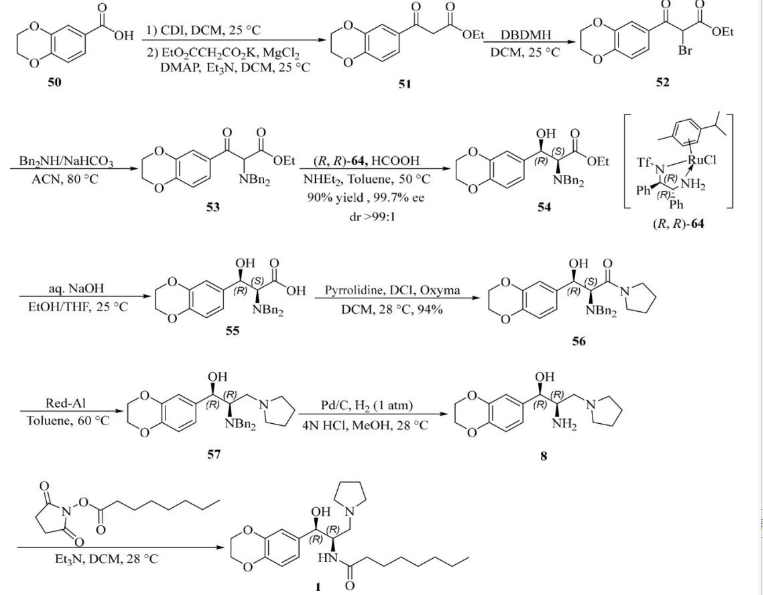
使用的所有试剂都很便宜,除了一种昂贵的钌催化剂(R,R)-64。钌催化剂可以回收并重复使用3次而不会失去活性。该方法适合大规模生产。
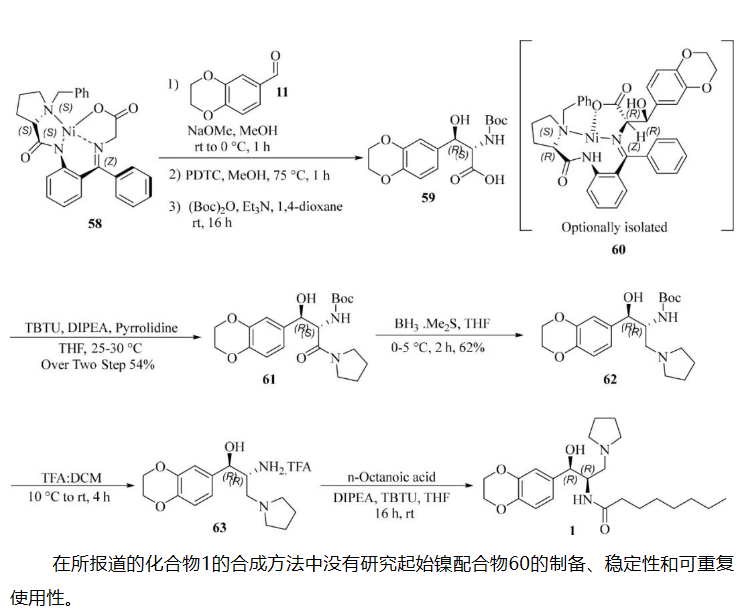
参考文献:
https://doi.org/10.1021/acs.oprd.3c00190